Nhóm oxit vừa tác dụng với nước, vừa tác dụng với dung dịch HCl là
A. N a 2 O , S O 3 , C O 2
B. K 2 O , P 2 O 5 , CaO
C. BaO, A l 2 O 3 , N a 2 O
D. CaO, BaO, K 2 O
Chất A có % các nguyên tố C, H, N, O lần lượt là 40,45%; 7,86%; 15,73%; còn lại là O. Khối lượng mol phân tử của A < 100. A vừa tác dụng với dung dịch NaOH vừa tác dụng với dung dịch HCl, có nguồn gốc thiên nhiên. CTCT của A là
A. NH2(CH2)3COOH.
B. NH2CH2COOH.
C. CH3-CH(NH2)-COOH.
D. NH2(CH2)2COOH.
Chất A có % các nguyên tố C, H, N, O lần lượt là 40,45%; 7,86%; 15,73%; còn lại là O. Khối lượng mol phân tử của A < 100. A vừa tác dụng với dung dịch NaOH vừa tác dụng với dung dịch HCl, có nguồn gốc thiên nhiên. CTCT của A là
A. NH2(CH2)3COOH
B. NH2CH2COOH
C. CH3-CH(NH2)-COOH
D. NH2(CH2)2COOH
Đáp án C
X là amino axit thiên nhiên => α => Loại A và D.
nC : nH : nN
= ![]()
Dãy oxit vừa tác dụng với nước, vừa tác dụng với dung dịch axit là:
A. C u O , F e 2 O 3 , S O 2 , C O 2 .
B. C a O , C u O , C O , N 2 O 5 .
C. C a O , N a 2 O , K 2 O , B a O .
D. S O 2 , M g O , C u O , A g 2 O .
Dãy oxit nào sau đây vừa tác dụng với nước, vừa tác dụng với dung dịch bazơ
A. CaO, CuO
B. CO, N a 2 O
C. C O 2 , S O 2
D. P 2 O 5 , MgO
Chọn C
Chất vừa tác dụng được với nước, vừa tác dụng được với dung dịch bazơ là oxit axit
=> C O 2 , S O 2 thỏa mãn
Câu 18: Cho 146 gam dung dịch HCl 50 % tác dụng vừa đủ với dung dịch Na2CO3 . Tìm thể tích khí sinh ra ở ĐKC (H=1, S=32 ,O=16 ,Na=23, C =12)
A. 44,8 l
B. 4,48 l
C. 22,4 l
D. 2,24 l
Câu 19: Cho 500 ml dung dịch NaOH 9 M tác dụng vừa đủ với dung dịch FeCl3. Tìm khối lượng kết tủa thu được sau phản ứng (Fe=56 ,O=16 ,H=1, Cl=35,5. Na=23)
A. 1,605 g
B. 16,05 g
C. 160,50 g
D. 96,3 g
Câu 20: Nhiệt phân hoàn toàn 174g Mg(OH)2. Tìm khối lượng chất rắn thu được sau phản ứng (Mg=24 ,O=16, H=1):
A. 120 g
B. 12 g
C. 6 g
D. 72 g
\(n_{HCl}=\dfrac{146.50}{100.36,5}=2\left(mol\right)\)
PTHH: Na2CO3 + 2HCl --> 2NaCl + CO2 + H2O
_______________2----------------->1
=> VCO2 = 1.22,4 = 22,4 (l)
=> C
Cho 4,8 magie oxit tác dụng vừa đủ với 200g dung dịch axit sunfuric loãng.Nồng độ % dung dịch thu được là(Biết Mg=24,S=32,H=1,O=16)
A. 7,20%
B. 7,30%
C. 7,03%
D. 2,40%
\(n_{Mg}=\dfrac{4,8}{40}=0,12\left(mol\right)\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\n_{MgO}=n_{MgSO_4}=0,12\left(mol\right)\\ m_{ddMgSO_4}=m_{Mg}+m_{ddH_2SO_4}=4,8+200=204,8\left(g\right)\\ m_{MgSO_4}=0,12.120=14,4\left(g\right)\\ C\%_{ddMgSO_4}=\dfrac{14,4}{204,8}.100\approx7,03\%\\ \Rightarrow C\)
Cho 10,2g nhôm oxit (Al2O3) tác dụng vừa đủ với dung dịch HCl 14,6%
a,Viết phương trình
b,Tính khối lượng dung dịch HCl
c,Tính nồng độ % của dung dịch sau phản ứng
nAl2O3=10.2:102=0.1(mol)
PTHH:Al2O3+6HCl->2AlCl3+3H2O
theo pthh:nHCl:nAl2O3=6->nHCl=6*0.1=0.6(mol)
mHCl=0.6*36.5=21.9(g)
mdd HCl=21.9*100:14.6=150(g)
theo pthh:nAlCl3:nAl2O3=2->nAlCl3=0.1*2=0.2(mol)
mAlCl3=0.2*133.5=26.7(g)
mdd sau phản ứng:10.2+150=160.2
C%=26.7:160.2*100=16.7%
Chất vừa tác dụng với dung dịch NaOH, vừa tác dụng với dung dịch HCl là
A. NaHCO3.
B. (NH4)2SO4
C. AlCl3
D. Na2CO3
Chất vừa tác dụng với dung dịch NaOH, vừa tác dụng với dung dịch HCl là
A. NaHCO3.
B. (NH4)2SO4.
C. AlCl3.
D. Na2CO3.
Đáp án A
A. Thỏa mãn vì:
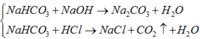
B. Loại vì không tác dụng được với HCl: (NH4)2SO4 + 2NaOH → Na2SO4 + 2NH3↑ + 2H2O.
C. Loại vì không tác dụng được với HCl: AlCl3 + 3NaOH → 3NaCl + Al(OH)3↓.
(Nếu NaOH dư thì Al(OH)3 + NaOH → NaAlO2 + 2H2O).
D. Loại vì không tác dụng được với NaOH: Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O.