Bài 21:Dung dịch X chứa 0,12 mol Mg2+; 0,1 mol Fe3+ ; a mol Cl- và b mol SO42-. Cô cạn X thu được 381,48 gam muối khan. Cho Ba(OH)2 dư vào X thu được m gam kết tủa. Giá trị của m là?
TL
Những câu hỏi liên quan
Dung dịch X chứa các ion: 0,1 mol Na+ ; 0,2 mol Ca2+ ; 0,3 mol Mg2+ ; 0,4 mol Cl‒ và x mol HCO3–. Đun sôi dung dịch X thu được dung dịch Y. Dung dịch Y là A. nước cứng toàn phần B. nước cứng vĩnh cửu C. nước mềm D. nước cứng tạm thời
Đọc tiếp
Dung dịch X chứa các ion: 0,1 mol Na+ ; 0,2 mol Ca2+ ; 0,3 mol Mg2+ ; 0,4 mol Cl‒ và x mol HCO3–. Đun sôi dung dịch X thu được dung dịch Y. Dung dịch Y là
A. nước cứng toàn phần
B. nước cứng vĩnh cửu
C. nước mềm
D. nước cứng tạm thời
Đáp án B
Bảo toàn điện tích: x=0,7 và x <0,2.2+0,3.2
do vậy đây là nước cứng vĩnh cửu
Đúng 0
Bình luận (0)
Dung dịch X chứa các ion: 0,1 mol Na+ ; 0,2 mol Ca2+ ; 0,3 mol Mg2+ ; 0,4 mol Cl‒ và x mol HCO3–. Đun sôi dung dịch X thu được dung dịch Y. Dung dịch Y là A. nước cứng toàn phần B. nước cứng vĩnh cửu C. nước mềm D. nước cứng tạm thời
Đọc tiếp
Dung dịch X chứa các ion: 0,1 mol Na+ ; 0,2 mol Ca2+ ; 0,3 mol Mg2+ ; 0,4 mol Cl‒ và x mol HCO3–. Đun sôi dung dịch X thu được dung dịch Y. Dung dịch Y là
A. nước cứng toàn phần
B. nước cứng vĩnh cửu
C. nước mềm
D. nước cứng tạm thời
Đáp án B
Bảo toàn điện tích: x=0,7 và x <0,2.2+0,3.2 do vậy đây là nước cứng vĩnh cửu
Đúng 0
Bình luận (0)
Dung dịch X có chứa 0,23 gam ion Na+; 0,12 gam ion Mg2+; 0,355 gam ion Cl- và m gam ion SO42-. Số gam muối khan sẽ thu được khi cô cạn dung dịch X là: A. 1,185 gam B. 1,19 gam C. 1,2 gam D. 1,158 gam
Đọc tiếp
Dung dịch X có chứa 0,23 gam ion Na+; 0,12 gam ion Mg2+; 0,355 gam ion Cl- và m gam ion SO42-. Số gam muối khan sẽ thu được khi cô cạn dung dịch X là:
A. 1,185 gam
B. 1,19 gam
C. 1,2 gam
D. 1,158 gam
Đáp án A
Định luật bảo toàn điện tích suy ra
nSO4(2-)=(0,01.1+ 5.10-3.2- 0,01)/2=0,005 mol
Khối lượng muối khan thu được là: 0,23+ 0,12+ 0,355+ 0,005.96= 1,185 gam
Đúng 0
Bình luận (0)
Dung dịch A chứa Na+ 0,1 mol, Mg2+ 0,05 mol, SO42- 0,04 mol còn lại là x mol Cl-. Tính khối lượng muối trong dung dịch
Theo bảo toàn điện tích có:
\(0,1.1+0,05.2=0,04.2+n_{Cl^-}\\ \Rightarrow n_{Cl^-}=0,12\left(mol\right)\)
Khối lượng muối trong dung dịch là:
\(m_{Na^+}+m_{Mg^{2+}}+m_{SO_4^{2-}}+m_{Cl^-}=23.0,1+24.0,05+0,04.96+0,12.35,5=11,6\left(g\right)\)
Đúng 1
Bình luận (0)
Dung dịch X chứa a mol NH4+ ; b mol Al3+; c mol Mg2+; x mol NO3– ; y mol SO42– . Mối quan hệ giữa số mol các ion trong dung dịch là A. a + b +c x + y B. a + 3b + 2c x + 2y C. a + b/3 + c/2 x + y/2 a + 2b +3c x + 2y
Đọc tiếp
Dung dịch X chứa a mol NH4+ ; b mol Al3+; c mol Mg2+; x mol NO3– ; y mol SO42– . Mối quan hệ giữa số mol các ion trong dung dịch là
A. a + b +c = x + y
B. a + 3b + 2c = x + 2y
C. a + b/3 + c/2 = x + y/2
a + 2b +3c = x + 2y
Chọn đáp án B
Bảo toàn điện tích: ∑nđiện tích (+) = ∑nđiện tích (-).
⇒ a + 3b + 2c = x + y ⇒ chọn B.
Đúng 0
Bình luận (0)
Dung dịch X chứa 0,1 mol Ca2+; 0,3 mol Mg2+; 0,4 mol Cl- và a mol HCO3-. Đun dung dịch X đến cạn thu được muối khan có khối lượng là A. 37,4 B. 23,2 C. 49,4 D. 28,6
Đọc tiếp
Dung dịch X chứa 0,1 mol Ca2+; 0,3 mol Mg2+; 0,4 mol Cl- và a mol HCO3-. Đun dung dịch X đến cạn thu được muối khan có khối lượng là
A. 37,4
B. 23,2
C. 49,4
D. 28,6
Đáp án A
Áp dụng định luật bảo toàn điện tích ta có:
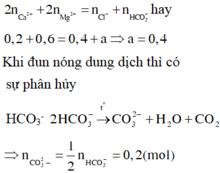
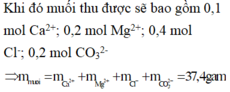
Đáp án A.
Đúng 0
Bình luận (0)
Dung dịch X chứa 0,2 mol
C
a
2
+
; a mol
M
g
2
+
; 0,3 mol
C
l
-
và 0,2 mol
H
C
O...
Đọc tiếp
Dung dịch X chứa 0,2 mol C a 2 + ; a mol M g 2 + ; 0,3 mol C l - và 0,2 mol H C O 3 - . Đun dung dịch X đến cạn thu được muối khan có khối lượng là
A. 37,4 gam
B. 49,4 gam
C. 25,85 gam
D. 33,25 gam
Đáp án C
Bảo toàn điện tích trong dung dịch
ta có 0,2.2 + 2a = 0,3 + 0,2
=>a = 0,05
Đun đến cạn dung dịch xảy ra phản ứng
HCO3- => H2O + CO2 + CO32-
n C O 3 2 - =0,1 mol
Vậy mmuối = 25,85 gam
Đúng 0
Bình luận (0)
Dung dịch X chứa 0,1 mol Ca2+; 0,3 mol Mg2+; 0,4 mol
Cl
-
và a mol
HNO
3
-
. Đun dung dịch X đến cạn thu được muối khan có khối lượng là A. 37,4 gam. B. 49,4 gam. C. 23,2 gam. D. 28,6 gam.
Đọc tiếp
Dung dịch X chứa 0,1 mol Ca2+; 0,3 mol Mg2+; 0,4 mol Cl - và a mol HNO 3 - . Đun dung dịch X đến cạn thu được muối khan có khối lượng là
A. 37,4 gam.
B. 49,4 gam.
C. 23,2 gam.
D. 28,6 gam.
Dung dịch X chứa 0,1 mol Ca2+; 0,3 mol Mg2+; 0,4 mol Cl- và a mol HCO3-. Đun dung dịch X đến cạn thu được muối khan có khối lượng là
A. 37,4 gam
B. 49,4 gam
C. 23,2 gam
D. 28,6 gam
Đáp án : A
Bảo toàn điện tích : 0,1.2 + 0,3.2 = 0,4 + a
=> a = 0,4 mol
2HCO3‑ -> CO32- + CO2 + H2O
=> sau phản ứng có 0,1 mol Ca2+ ; 0,3 mol Mg2+ ; 0,2 mol CO32- và 0,4 mol Cl-
=> mmuối khan = 37,4g
Đúng 0
Bình luận (0)
Dung dịch X chứa 0,1 mol
C
a
2
+
; 0,3 mol
M
g
2
+
, 0,4 mol
C
l
-
và a mol
H
C
O
3
-
. Đun dung dịch X đến cô cạn thu được muối khan có khối lượng là A. 49,4 gam B.28,6 gam C. 37,4 ga...
Đọc tiếp
Dung dịch X chứa 0,1 mol C a 2 + ; 0,3 mol M g 2 + , 0,4 mol C l - và a mol H C O 3 - . Đun dung dịch X đến cô cạn thu được muối khan có khối lượng là
A. 49,4 gam
B.28,6 gam
C. 37,4 gam
D. 23,2 gam




