Phân biệt sự oxi hoá, sự cháy và sự oxi hóa chậm. Cho ví dụ.
QA
Những câu hỏi liên quan
a.Phản ứng hóa hợp, phản ứng phân hủy là gì? Lấy ví dụ
b. Sự oxi hóa là gì? Sự cháy là gì, sự oxi hóa chậm là gì? Lấy ví dụ
c . Nêu thành phần không khí, nguyên nhân gây ô nhiễm không khí, các biện pháp bảo vệ không khí trong lành.
d. Nêu điều kiện phát sinh và các biện pháp dập tắt đám cháy.
câu a:
phản ứng hóa hợp là: pứ Có 2 hoặc nhìu hợp chất tham gia chỉ tạo ra 1 hợp chất sp.
\(4K+O_2\underrightarrow{t^o}2K_2O\)
phản ứng phân hủy là : pứ chỉ có 1 chất nhưng tạo ra 2 hoặc nhiều chất.
\(2KMnO_4\rightarrow MnO_2+K_2MnO_4+O_2\uparrow\)
câu b:
--->Sự oxi hóa là sự tác dụng của oxi với một chất (chất đó có thể là đơn chất hoặc hợp chất).
- Ví dụ: Sự oxi hóa cacbon
câu c
-->Sự cháy là sự oxi hóa có tỏa nhiệt và phát sáng.
Ví dụ: Nến cháy, khí gas cháy,...
----Sự oxi hóa chậm là :
+ sự oxi hóa có tỏa nhiệt nhưng không phát sáng.
+ thường xảy ra trong tự nhiên như các đồ vật bằng gang sắt thép trong tự nhiên dần dần biến đổi thành sắt oxit.
Sự oxi hóa chậm các chất hữu cơ trong cơ thể luôn diễn ra và tạo ra năng lượng đó giúp cơ thể hoạt động được
Đúng 1
Bình luận (0)
Chỉ ra quá trình khác biệt với 3 quá trình còn lại: sự cháy, sự quang hợp, sự hô hấp, sự oxi hoá chậm?
A. Sự cháy.
B. Sự quang hợp.
C. Sự hô hấp.
D. Sự oxi hoá chậm.
Chọn đáp án B
+ sự cháy, sự hô hấp, sự oxi hoá đều cần Oxi
+ còn sự quang hợp sinh ra Oxi.
Đúng 0
Bình luận (0)
nêu các khái niệm sự oxi hóa phản ứng hóa hợp, phản ứng phân hủy, sự cháy, sự oxi hóa chậm, phản ứng thế
Các khái niệm sự oxi hóa phản ứng hóa hợp, phản ứng phân hủy, sự cháy, sự oxi hóa chậm, phản ứng:
- Sự oxi hóa là sự tác dụng của oxi với một chất (chất đó có thể là đơn chất hoặc hợp chất).
- Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
- Phản ứng phân hủy là một phản ứng hóa học mà trong đó một chất tham gia có thể tạo thành hai hay nhiều chất mới.
- Sự cháy là phản ứng oxy hóa khử nhiệt độ cao giữa chất đốt và chất oxy hóa, có sinh ra ngọn lửa sáng
- Sự oxi hóa chậm là sự oxi hóa có tỏa nhiệt nhưng không phát sáng.
- Phản ứng thế là phản ứng hóa học, trong đó một nguyên tố có độ hoạt động hóa học mạnh sẽ thay thế cho nguyên tố có độ hoạt động hóa học yếu hơn trong hợp chất của nguyên tố này
Đúng 0
Bình luận (0)
Câu 3: Sự cháy và sự oxi hoá chậm có điểm chung là đều
A. toả nhiệt và phát sáng
B. toả nhiệt và không phát sáng.
C. xảy ra sự oxi hoá và có toả nhiệt.
D. xảy ra sự oxi hoá và không phát sáng.
C.
Điểm giống nhau giữa sự cháy và sự oxi hóa chậm: đều là sự oxi hóa có tỏa nhiệt.
Điểm khác nhau giữa sự cháy và sự oxi hóa chậm: sự oxi hóa chậm không phát sáng còn sự cháy có phát sáng.
Đúng 1
Bình luận (0)
C. xảy ra sự oxi hoá và có toả nhiệt.
![]()
![]()
![]()
Đúng 0
Bình luận (0)
Phân biệt chất oxi hóa và sự oxi hóa, chất khử và sự khử. Lấy thí dụ để minh họa.
Chất oxi hóa là chất nhận electron.
Sự oxi hóa một chất là làm cho chất đó nhường electron.
Chất khử là chất nhường electron.
Sự khử một chất là sự làm cho chất đó thu electron.
Thí dụ: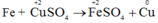
- Nguyên tử Fe nhường electron, là chất khử. Sự nhường electron của Fe được gọi là sự oxi hóa nguyên tử sắt.
- Ion đồng nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Đúng 0
Bình luận (0)
điểm giống và khác nhau giữa sự cháy và sự oxi hoá chậm là j ?
| Sự cháy | Sự oxi hóa chậm | |
| Giống nhau | - Đều là sự oxi hóa có tỏa nhiệt | - Đều là sự oxi hóa có tỏa nhiệt |
| Khác nhau | - Có phát sáng | - Không phát sáng |
Đúng 2
Bình luận (0)
Sự cháy và sự oxi hóa chậm có đặc điểm chung là:
A. Tỏa nhiệt và phát sáng.
B. Tỏa nhiệt nhưng không phát sáng.
C. Xảy ra sự oxi hóa và có tỏa nhiệt.
D. Xảy ra sự oxi hóa nhưng không phát sáng.
Sự cháy và sự oxi hóa chậm có đặc điểm chung là:
A. Tỏa nhiệt và phát sáng.
B. Tỏa nhiệt nhưng không phát sáng.
C. Xảy ra sự oxi hóa và có tỏa nhiệt.
D. Xảy ra sự oxi hóa nhưng không phát sáng.
⇒ Đáp án: C. Xảy ra sự oxi hóa và có tỏa nhiệt.
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Sự giống nhau giữa sự cháy và sự oxi hóa chậm là
A. Phát sáng
B. Cháy
C. Tỏa nhiệt
D. Sự oxi hóa xảy ra chậm
1) Quá trình oxi hóa (sự oxi hóa) là gì? Cho ví dụ
2) Quá trình khử (sự khử) là gì? Cho ví dụ1/ Quá trình khử là quá trình nhường electron của một chất.
Ví dụ Trong phản ứng: Fe + 2HCl -> FeCl2 + H2 thì Fe đã bị khử thành Fe (+2)
2/ Quá trình oxy hoá là quá trình nhận electron của một chất.
Ví dụ: cũng trong phản ứng trên, H+ bị oxi hoá thành H2
Đúng 0
Bình luận (0)
Phân biệt chất oxi hoá và sự oxi hoá, chất khử và sự khử. Lấy thí dụ để minh họa.
Chất oxi hoá là chất nhận electron.
Sự oxi hoá một chất là làm cho chất đó nhường electron.
Chất khử là chất nhường electron.
Sự khử một chất là sự làm cho chất đó thu electron.
Thí dụ: Fe + CuSO4 → FeSO4 + Cu
- Nguyên tử Fe nhường elcctron, là chất khử. Sự nhường electron của Fe được gọi là sự oxi hoá nguyên tử sắt.
- Ion đồng nhận electron, là chất oxi hoá. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Đúng 0
Bình luận (0)






