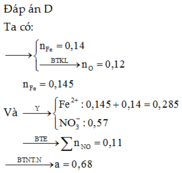
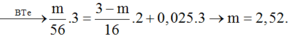Đốt m gam bột sắt trong khí oxi thu được 7,36 gam chất rắn X gồm: Fe; FeO; Fe3O4; Fe2O3. Để hoà tan hoàn toàn hỗn hợp X cần vừa hết 120 ml dung dịch H2SO4 1M ( loãng), tạo thành 0,224 l H2 ở đktc.
A.Viết phương trình hoá học xảy ra.
B. Tính m?
Cho Fe = 56, O = 16, Ca = 40, S = 32, C = 12, H = 1