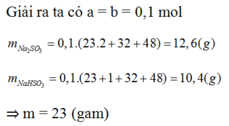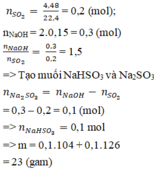Hấp thụ 4,48l SO2 (đktc) vào 150ml dung dịch NaOH 2M thu đc dung dịch chứ m gam muối tính m
HC
Những câu hỏi liên quan
Hấp thụ 4,48 lít SO2 (đktc) vào 150ml dung dịch NaOH 2M, thu được dung dịch chứa m gam muối. Giá trị của m là:
A. 18,9
B. 25,2
C. 20,8
D. 23,0
Câu 6: Hấp thụ 4,48 lít SO2 (đktc) vào 150 ml dung dịch NaOH 2M, thu được dung dịch chứa m gam muối. Tính giá trị của m
nSO2 = 4.48/22.4 = 0.2 (mol)
nNaOH = 0.15*2 = 0.3 (mol)
nNaOH / nSO2 = 0.3 / 0.2 = 1.5
=> Tạo ra 2 muối
Đặt :
nNa2SO3 = x mol
nNaHSO3 = y mol
=> 2x + y = 0.3
x + y = 0.2
=> x = y = 0.1
mNa2SO3 = 0.1*126 = 12.6 (g)
mNaHSO3 = 0.1*104 = 10.4 (g)
Đúng 2
Bình luận (0)
nNaOH= 0,3(mol); nSO2=0,2(mol)
Ta có: 2>nOH-/nSO2=0,3/0,2=1,5>1
=> Sản phẩm là hỗn hợp 2 muối: Na2SO3 và NaHSO3
PTHH: 2 NaOH + SO2 -> Na2SO3 + H2O
2x____________x_____x(mol)
NaOH + SO2 -> NaHSO3
y_______y______y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}x+y=0,2\\2x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
=> m(muối)=mNa2SO3+ mNaHSO3= 126x+104y=126.0,1+104.0,1=23(g)
Đúng 2
Bình luận (0)
Hấp thụ 4,48 lít SO 2 (đktc) vào 150 ml dung dịch NaOH 2M, thu được dung dịch chứa m gam muối. Giá trị của m là
A. 18,9
B. 25,2
C. 20,8
D. 23,0
Hấp thụ hoàn toàn 4,48 lít khí SO2 (đktc) vào dung dịch chứa 16g NaOH thu được dung dịch X. Khối lượng muối tan thu được trong dung dịch X là:C. 23,0g A. 20,8g D. 25,2 gam B. 18,9 gamCâu 10: Sục V lít CO2 (đktc) vào 150ml dung dịch Ba(OH)2 1M, sau phản ứng thu được 19,7g kết tủa. Giá trị của V là:A. 2,24 lít; 4,48 lít B. 2,24 lít; 3,36 lít C. 3,36 lít; 2,24 lít D. 22,4 lít; 3,36 lítCâu 11: Sục 2,24 lít CO2 (đktc) vào 750ml dung dịch NaOH 0,2M. Số mol của Na2CO3 và NaHCO3 là:D. 0,07 và 0,05 A. 0,...
Đọc tiếp
Hấp thụ hoàn toàn 4,48 lít khí SO2 (đktc) vào dung dịch chứa 16g NaOH thu được dung dịch X. Khối lượng muối tan thu được trong dung dịch X là:
C. 23,0g A. 20,8g D. 25,2 gam B. 18,9 gam
Câu 10: Sục V lít CO2 (đktc) vào 150ml dung dịch Ba(OH)2 1M, sau phản ứng thu được 19,7g kết tủa. Giá trị của V là:
A. 2,24 lít; 4,48 lít B. 2,24 lít; 3,36 lít C. 3,36 lít; 2,24 lít D. 22,4 lít; 3,36 lít
Câu 11: Sục 2,24 lít CO2 (đktc) vào 750ml dung dịch NaOH 0,2M. Số mol của Na2CO3 và NaHCO3 là:
D. 0,07 và 0,05 A. 0,05 và 0,05 B. 0,06 và 0,06 C. 0,05 và 0,06
Câu 12: Dẫn 10 lít hỗn hợp khí gồm N2 và CO2 (đktc) sục vào 2 lít dung dịch Ca(OH)2 0,02M thu được 1g kết tủa. Tính phần trăm theo thể tích CO2 trong hỗn hợp khí:
C. 2,24% và 15,86% A. 2,24% và 15,68% B. 2,4% và 15,68% D. 2,8% và 16,68%
9
nSO2 = 4,48 : 22,4 = 0,2 (mol) ; nNaOH = 16: 40 = 0,4 (mol)
Ta thấy nNaOH/ nSO2 = 2 => chỉ tạo muối Na2SO3
=> mNa2SO3 = 0,2. 126 = 25, 2(g) =>D
10
nBa(OH) = 0,15.1 = 0,15mol; nBaCO3 = 19,7 : 197 = 0,1mol
Vì nBaCO3 < nBa(OH)2 → xét 2 trường hợp
Trường hợp 1: Ba(OH)2 dư, CO2 hết, phản ứng chỉ tạo muối cacbonat
CO2 + Ba(OH)2 → BaCO3 + H2O
0,1 0,1
Vậy V = VCO2 = 0,1.22,4 =2,24
Trường hợp 2: Phản ứng sinh ra 2 muối cacbonat và hiđrocacbonat
CO2 + Ba(OH)2→ BaCO3 + H2O (1)
0,1 0,1 0,1
2CO2+Ba(OH)2→Ba(HCO3)2
0,1 0,05
Theo phương trình (1): nBa(OH)2(1) = nBaCO3=0,1mol
Mà nBa(OH)2= 0,15mol →nBa(OH)2 (2) = 0,15−0,1 = 0,05mol
Theo (1) và (2): nCO2 = nBaCO3 + 2nBa(OH)2 (2) = 0,1 + 2.0,05 = 0,2 mol
Vậy V = VCO2 = 0,2.22,4 = 4,48 lít
=>A
Đúng 1
Bình luận (0)
Hấp thụ hoàn toàn 4,48 lít khí SO2 (ở đktc) vào dung dịch chứa m gam NaOH thu được dung dịch X chứa 23 gam hỗn hợp muối tan. Tìm gía trị của m.
Gọi $n_{NaHSO_3} = a(mol) ; n_{Na_2SO_3} = b(mol)$
$\Rightarrow 104a + 126b = 23(1)$
$NaOH + SO_2 \to NaHSO_3$
$2NaOH + SO_2 \to Na_2SO_3 + H_2O$
$n_{SO_2} = a + b = \dfrac{4,48}{22,4} = 0,2(2)$
Từ (1)(2) suy ra a = b = 0,1
$n_{NaOH} = a + 2b = 0,3(mol)$
$m = 0,3.40 = 12(gam)$
Đúng 3
Bình luận (0)
Hấp thụ hoàn toàn 6,72 lít SO2 (đktc) vào V lít dung dịch NaOH 2M thu được dung dịch X. Cô cạn X thu được 45,8 gam chất rắn. Tính V
\(m_{SO_2}=\dfrac{6,72}{22,4}.80=24\left(g\right)\)
AD ĐLBTKL ta có :
\(m_{SO_2}+m_{NaOH}=m_{NaHSO_3}\\ \Leftrightarrow m_{NaOH}=45,8-24=21,8\left(g\right)\)
\(\Rightarrow n_{NaOH}=21,8:40=0,07\left(mol\right)\)
\(V_{NaOH}=0,07:2=0,035\left(l\right)\)
Đúng 1
Bình luận (0)
Hấp thụ hoàn toàn 4,48 lít khí S O 2 (đktc) vào dung dịch chứa 16 gam NaOH thu được dung dịch X. Khối lượng muối tan thu được trong dung dịch X là
A. 25,2 gam.
B. 23,0 gam.
C. 18,9 gam.
D. 20,8 gam.
Hấp thụ hoàn toàn 4,48 lít khí SO2 (ở đktc) vào dung dịch chứa 16 gam NaOH, thu được dung dịch X. Khối lượng muối thu được trong dung dịch X là A. 25,2 gam B. 23,0 gam C. 20,8 gam D. 18,9 gam
Đọc tiếp
Hấp thụ hoàn toàn 4,48 lít khí SO2 (ở đktc) vào dung dịch chứa 16 gam NaOH, thu được dung dịch X. Khối lượng muối thu được trong dung dịch X là
A. 25,2 gam
B. 23,0 gam
C. 20,8 gam
D. 18,9 gam
Đáp án A
nSO2 = 0,2 mol
n NaOH = 0,4 mol
k = nNaOH/nSO2 = 0,4/0,2=2
k=2 => pứ tạo 1 muối trung hòa.
PT:
SO2 + 2NaOH → Na2SO3+H2O
0.2----0.4------->0.2
mNa2SO3 = 126.0.2 = 25.2g
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 4,48 lít khí SO2 ( ở đktc) vào dung dịch chứa 16 gam NaOH, thu được dung dịch X. Khối lượng muối tan thu được trong dung dịch X là
A. 18,9 gam.
B. 23,0 gam.
C. 20,8 gam.
D. 25,2 gam.
Đáp án D
nSO2 = 4,48 : 22,4 = 0,2 (mol) ; nNaOH = 16: 40 = 0,4 (mol)
Ta thấy nNaOH/ nSO2 = 2 => chỉ tạo muối Na2SO3
=> mNa2SO3 = 0,2. 126 = 25, 2(g)
Đúng 0
Bình luận (0)