Potassium sulfate có CTHH là k2SO4. CTHH trên cho biết điều gì
Mike cần gấp ạ
Potassium sulfate có CTHH là k2SO4. CTHH trên cho biết điều gì
Mike cần gấp ạ
CTHH K2SO4 cho biết
- K2SO4 do 3 nguyên tố: K, S và O tạo ra.
- K2SO4 gồm 2 nguyên tử K, 1 nguyên tử S và 4 nguyên tử O.
- Phân tử khối = 39.2 + 32 + 16.4 = 174
Giúp mình với . Nguyên tử R có tổng số hạt là 21, trong đó hạt mang điện chiếm 66,67% a, Tìm số hạt p,n,e.B, Hãy tìm khối lượng nguyên tử và cho biết tên.v,Vẽ cấu tạo nguyên tử nguyên tố R
Theo bài ra ta có
p+e+n=21
p+e=66,67%.21
Mà p=e
⇌2p+n=21
2p=66,67%
⇒p=e=7
n=7
Vậy R là nguyên tử nitrogen
+7)2)5
tổng số hạt trong nguyên tử x là 40. biết số hạt neutron lớn hơn proton 1 hạt. tính số hạt proton và electron
Ta có p+e+n=40
n-p=1
Mà p=e
→2p+n=40
Giải p=13=e
Nguyên tử Y có 3 lớp electron và có 7 electron lớp ngoài cùng
a. Vẽ mô hình nguyên tử Y
b. Xác định số proton, neutron, electron của Y. Biết số neutron nhiều hơn số proton là 1.
a) Sơ đồ nguyên tử Y là:
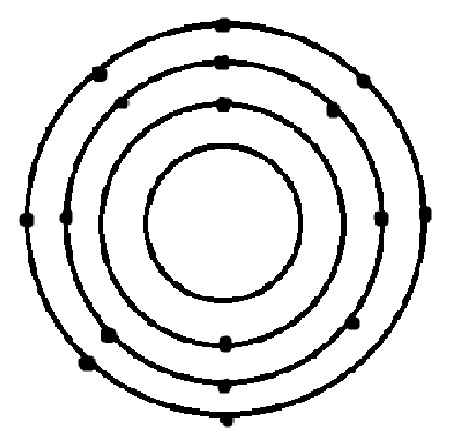
b)Vì nguyên tử Y có 3 lớp electron
Ta đã được biết: Lớp electron thứ nhất của mỗi nguyên tử sẽ có tối đa 2 electron
Lớp electron thứ hai của mỗi nguyên tử sẽ có tối đa 8 electron
Nên nguyên tử Y có số electron là:2+8+7=17(hạt)
Vì số electron và proton của mỗi nguyên tử đều bằng nhau
nên số proton =số electron = 17 (hạt)
Theo đề bài ta có:Số hạt neutron hơn số hạt electron là 1 hạt
nên số hạt neutron= số hạt proton + 1 =17+1=18 (hạt)
Câu 1:
a, \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
b, \(2Na+S\underrightarrow{t^o}Na_2S\)
c, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
d, \(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\)
e, \(Ca+Cl_2\underrightarrow{t^o}CaCl_2\)
Câu 2:
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
c, \(2Zn+O_2\underrightarrow{t^o}2ZnO\)
d, \(Cu+Cl_2\underrightarrow{t^o}CuCl_2\)
e, \(2K+S\underrightarrow{t^o}K_2S\)
Câu 3:
(1) \(Mg+CuCl_2\rightarrow MgCl_2+Cu\)
(2) \(2Cu+O_2\underrightarrow{t^o}2CuO\)
(3) \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
(4) \(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\)
(5) \(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
(6) \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Câu 4:
a, - Hiện tượng: Tạo thành khói màu nâu đỏ.
PT: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
b, - Hiện tượng: Màu xanh của dd nhạt dần, có kim loại Cu màu đỏ bám vào đinh sắt.
PT: \(Fe+CuCl_2\rightarrow FeCl_2+Cu\)
c, Không hiện tượng do không có pư xảy ra.
d, - Hiện tượng: Màu xanh dd nhạt dần, có bọt khí, có tủa màu xanh xuất hiện.
PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(2NaOH+CuSO_4\rightarrow Na_2SO_4+Cu\left(OH\right)_{2\downarrow}\)
Câu 5:
a, - Tác dụng với HCl: Na, Fe, Al, Mg
PT: \(2Na+2HCl\rightarrow2NaCl+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
- Tác dụng với NaOH: Al
PT: \(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
b, Na: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
c, Cu
d, Fe, Al, Mg
PT: \(Fe+CuCl_2\rightarrow FeCl_2+Cu\)
\(2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\)
\(Mg+CuCl_2\rightarrow MgCl_2+Cu\)
Phần 2:
C1: C
C2: D
C3: D
C4: B
Tổng số hạt trong một nguyên tử x là 28,trong đó số hạt không mang điện là 10
a) Tìm số p,e,n trong x
b) Vẽ cấu tạo của x
c) Cho biết tên và khối lượng của x
SOS mấy ní ơi
a,Theo bài ra, ta có:
\(\left\{{}\begin{matrix}2Z+N=28\\N=10\end{matrix}\right.\)
\(=>\left\{{}\begin{matrix}Z=E=9\\N=10\end{matrix}\right.\)
b,
,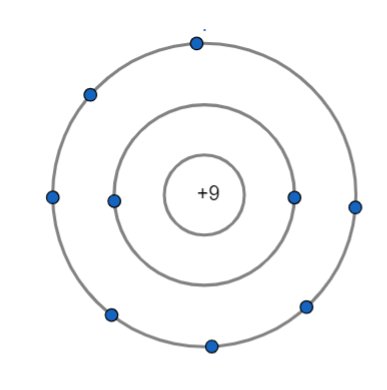
c, Tên: Fluorine ( F )
\(m_F=9+10=19\left(amu\right)\)
Mọi người ai biết cách xác định công thức hóa học của hợp chất khi biết phần trăm khối lượng các nguyên tố và khối lượng phân tử của hợp chất với dãy tỉ số bằng nhau không? Chỉ mình với ạ!!!
TK:
Có, bạn có thể sử dụng phương pháp phân tích phần trăm khối lượng để xác định công thức hóa học của một hợp chất khi biết phần trăm khối lượng của các nguyên tố và khối lượng phân tử của hợp chất. Điều này được gọi là phân tích phần trăm khối lượng hoặc phân tích phần trăm khối lượng.
Để sử dụng phương pháp này, bạn cần biết phần trăm khối lượng của mỗi nguyên tố trong hợp chất và khối lượng phân tử của hợp chất đó. Sau đó, bạn cần chia phần trăm khối lượng của mỗi nguyên tố cho khối lượng nguyên tử tương ứng của nguyên tố đó. Số lượng này gần đúng với số lượng nguyên tử của nguyên tố trong một phân tử của hợp chất.
Bằng cách so sánh các tỉ số này, bạn có thể xác định công thức hóa học của hợp chất. Nếu tỉ số gần đúng bằng nhau, đó có thể là công thức chính xác. Tuy nhiên, nếu tỉ số không chính xác, bạn có thể cần phải làm tròn hoặc điều chỉnh chúng để có được một công thức hợp lý.
Ví dụ, nếu bạn biết rằng một hợp chất có 40% carbon, 6.67% hydrogen, và 53.33% oxygen theo khối lượng và khối lượng phân tử của hợp chất đó là 90 g/mol, bạn có thể sử dụng phương trình sau:
1. Chia phần trăm khối lượng của mỗi nguyên tố cho khối lượng nguyên tử tương ứng của nó:
- Carbon: 40% / 12 g/mol ≈ 3.33
- Hydrogen: 6.67% / 1 g/mol ≈ 6.67
- Oxygen: 53.33% / 16 g/mol ≈ 3.33
2. So sánh các tỉ số này để xác định công thức hóa học. Trong trường hợp này, tỉ số cho carbon và oxygen là gần bằng nhau, vậy có thể hợp chất này là \( C_3H_7O_2 \).
Tuy nhiên, cần lưu ý rằng phương pháp này không phải lúc nào cũng đem lại kết quả chính xác và đôi khi có thể cần thêm thông tin bổ sung hoặc sử dụng các phương pháp phân tích khác để xác định công thức hóa học một cách chính xác hơn.
để di hỏi lại tui năm lớp 7 làm kiủ j đc 9,8 KHTN cái :))
Có cách nào để biết hoá trị qua khối lượng mol không ạ? VD oxygen thì mình có thể suy ra hoá trị khi biết O = 16 không ạ?
bảng tuần hoàn có mặt sau ghi hóa trị đó bn
Những chất sau đây được tạo bởi những nguyên tố hóa học nào ? số nguyên tử của mỗi nguyên tố ? NaCl ; Fe2(SO4)2 ; H3PO4 ; Na3PO4 ; Al(OH)3 .
Mai thi :((
$-$ NaCl: Gồm 2 nguyên tố là Natri (Na) và Clo (Cl) với số nguyên tử tương ứng là 1 và 1.
$-$ Fe2(SO4)2: Gồm 3 nguyên tố là Sắt (Fe), Lưu huỳnh (S) và Oxy (O) với số nguyên tử tương ứng là 2, 2 và 8.
$-$ H3PO4: Gồm 3 nguyên tố là Hydro (H), Photpho (P) và Oxy (O) với số nguyên tử tương ứng là 3, 1 và 4.
$-$ Na3PO4: Gồm 3 nguyên tố là Natri (Na), Photpho (P) và Oxy (O) với số nguyên tử tương ứng là 3, 1 và 4.
$-$ Al(OH)3: Gồm 3 nguyên tố là Nhôm (Al), Oxy (O) và Hydro (H) với số nguyên tử tương ứng là 1, 3 và 3.
một hợp chất gồm 1 nguyên tử x liên kết 1 nguyên tố O và ngặn gấp 2 lần phân tử nitrogen do 1 nguyên tử niter tạo ra tìm ra tên nguyên tố x ghi công thức nx nha
CT(X) \(XO\)
\(M_{XO}=2.14=28\\ \Rightarrow X+16=28\\ \Rightarrow X=12g/mol\)
=> X là Carbon
\(CY:CO\)