`#3107.101107`
`6.`
`a.`
PTHH: \(\text{Fe}_2\text{O}_3+3\text{H}_2\rightarrow\text{2Fe + 3H}_2\text{O}\)
`b.`
Số mol của Fe thu được trong pứ trên là:
\(\text{n}_{\text{Fe}}=\dfrac{\text{m}_{\text{Fe}}}{\text{M}_{\text{Fe}}}=\dfrac{11,2}{56}=0,2\left(\text{mol}\right)\)
Theo PT: `1` mol Fe2O3 thu được `2` mol Fe
`=> 0,1` mol Fe2O3 thu được `0,2` mol Fe
Khối lượng mol của Fe2O3 là:
\(\text{M}_{\text{Fe}_2\text{O}_3}=\text{M}_{Fe}\cdot2+\text{M}_{\text{O}}\cdot3=56\cdot2+16\cdot3=160\text{ (g/mol)}\)
Khối lượng của Fe2O3 có trong pứ trên là:
\(\text{m}_{\text{Fe}_2\text{O}_3}=\text{n}_{\text{Fe}_2\text{O}_3}\cdot\text{M}_{\text{Fe}_2\text{O}_3}=0,1\cdot160=16\left(g\right)\)
Vậy, m của Fe2O3 có trong pứ trên là `16` g.
_____
Theo PT: `3` mol H2 thu được `2` mol Fe
`=> 0,3` mol H2 thu được `0,2` mol Fe
Thể tích của khí H2 trong pứ trên là:
\(\text{V}_{\text{H}_2}=\text{n}_{\text{H}_2}\cdot24,79=0,2\cdot24,79=4,958\left(l\right)\)
Vậy, V của H2 trong pứ trên là `4,958` l.





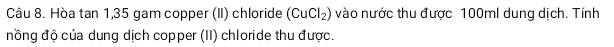





 Giải hết và chi tiết với ạ. Em đang cần gấp ạ. Em cảm ơn nhiều ạ.
Giải hết và chi tiết với ạ. Em đang cần gấp ạ. Em cảm ơn nhiều ạ.