Thí nghiệm 1: sục 6,72 lít khí CO2 vào dung dịch chứa a mol Ca(OH)2 thu được 3b mol kết tủa. Thí nghiệm 2: sục 11,2 lít khí CO2 vào dung dịch chứa a mol Ca(OH)2 thu được 3,5b mol kết tủa. Hãy tìm a và b
Chương 3. Nhóm cacbon
Ta có: \(\left\{{}\begin{matrix}n_{Ca\left(OH\right)_2\left(TN_1\right)}=n_{Ca\left(OH\right)_2\left(TN_2\right)}\\V_{CO_2\left(TN_1\right)}< V_{CO_2\left(TN_2\right)}\\n_{kt\left(TN_1\right)}< n_{kt\left(TN_2\right)}\end{matrix}\right.\)
=> Ở TN1 Ca(OH)2 dư
- TN1: \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,3------>0,3
=> 3b = 0,3 => b = 0,1
- TN1: \(\left\{{}\begin{matrix}n_{CaCO_3}=3,5.0,1=0,35\left(mol\right)\\n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\end{matrix}\right.\)
Vì \(n_{C\left(CO_2\right)}>n_{C\left(CaCO_3\right)}\left(0,5>0,35\right)\) => Kết tủa đã tan ra một phần
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
\(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
BTNT C: \(n_{Ca\left(HCO_3\right)_2}=\dfrac{n_{CO_2}-n_{CaCO_3}}{2}=0,075\left(mol\right)\)
BTNT Ca: \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}=0,425\left(mol\right)\)
Hay a = 0,425
Đúng 1
Bình luận (0)
Cho V lít dung dịch Ca(OH)2 1M. Thí nghiệm 1: sục 6,72 lít khí CO2 vào V lít dung dịch Ca(OH)2 thu được 4b mol kết tủa. Thí nghiệm 2: sục 8,96 lít khí CO2 vào V lít dung dịch Ca(OH)2 thu được 2b mol kết tủa. Hãy tìm V và b.
Vì ở 2 thí nghiệm Ca(OH)2 như nhau
Ở TN2 nhiều CO2 hơn
Ở TN2 ít kết tủa hơn
=> Ở TN2 CO2, kết tủa đã tan ra một phần
- TN1: \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
- TN2: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\) (1)
\(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\) (2)
Theo PT (2): \(n_{CaCO_3}=n_{CO_2}\)
=> \(n_{CaCO_3\left(tan.ra\right)}=n_{CO_2\left(thêm.vào\right)}\)
=> 4b - 2b = 0,4 - 0,3 => b = 0,05
- TN2: \(n_{CaCO_3}=0,05.2=0,1\left(mol\right)\)
BTNT C: \(n_{Ca\left(HCO_3\right)_2}=\dfrac{n_{CO_2}-n_{Ca\left(HCO_3\right)_2}}{2}=0,15\left(mol\right)\)
BTNT Ca: \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}=0,25\left(mol\right)\)
=> \(V=V_{ddCa\left(OH\right)_2}=\dfrac{0,25}{1}=0,25\left(l\right)\)
Đúng 2
Bình luận (0)
Hấp thụ hoàn toàn 1,344 lít CO2 (đktc) vào 500 ml dung dịch gồm NaOH 0,1M và KOH 0,06M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X. Thêm 250 ml dung dịch Y gồm BaCl2 0,16M và Ba(OH)2 aM vào X thu được 5,91 gam kết tủa. Giá trị của a
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\\n_{OH^-}=0,5.\left(0,1+0,06\right)=0,08\left(mol\right)\\n_{BaCl_2}=0,25.0,16=0,04\left(mol\right)\\n_{BaCO_3}=\dfrac{5,91}{197}=0,03\left(mol\right)\end{matrix}\right.\)
PT ion rút gọn: \(CO_2+2OH^-\rightarrow CO_3^{2-}+H_2O\) (1)
0,04<---0,08------->0,04
\(CO_3^{2-}+CO_2+H_2O\rightarrow2HCO_3^-\) (2)
0,02<---0,02-------------->0,04
=> dd X có \(\left\{{}\begin{matrix}n_{CO_3^{2-}}=0,02\left(mol\right)\\n_{HCO_3^-}=0,04\left(mol\right)\end{matrix}\right.\)
Ta có: \(n_{BaCO_3}< n_{BaCl_2}\left(0,03< 0,04\right)\)
=> Ba2+ dư, CO32- hết
PT ion rút gọn: \(OH^-+HCO_3^{2-}\rightarrow CO_3^{2-}+H_2O\) (3)
\(Ba^{2+}+CO_3^{2-}\rightarrow BaCO_3\downarrow\) (4)
0,03<-----0,03
=> \(n_{CO_3^{2-}\left(3\right)}=0,03-0,02=0,01\left(mol\right)\)
Theo (3): \(n_{OH^-}=n_{CO_3^{2-}}=0,01\left(mol\right)\)
=> \(n_{Ba\left(OH\right)_2}=\dfrac{1}{2}n_{OH^-}=0,005\left(mol\right)\)
=> \(a=C_{M\left(Ba\left(OH\right)_2\right)}=\dfrac{0,005}{0,25}=0,02M\)
Đúng 1
Bình luận (0)
Hấp thụ hoàn toàn 8,96 lít CO2 (đktc) vào 500 ml dung dịch gồm NaOH 0,5M và KOH 0,5M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y. Chia Y làm 2 phần bằng nhauCho 1/2 Y tác dụng với dung dịch Ba(OH)2 (dư), thu được a gam kết tủa.Cho 1/2 Y tác dụng với dung dịch BaCl2 (dư), thu được b gam kết tủa.Giá trị của (a-b) là:
Đọc tiếp
Hấp thụ hoàn toàn 8,96 lít CO2 (đktc) vào 500 ml dung dịch gồm NaOH 0,5M và KOH 0,5M, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y. Chia Y làm 2 phần bằng nhau
Cho 1/2 Y tác dụng với dung dịch Ba(OH)2 (dư), thu được a gam kết tủa.
Cho 1/2 Y tác dụng với dung dịch BaCl2 (dư), thu được b gam kết tủa.
Giá trị của (a-b) là:
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\n_{OH^-}=0,5.\left(0,5+0,5\right)=0,5\left(mol\right)\end{matrix}\right.\)
PT: \(2OH^-+CO_2\rightarrow CO_3^{2-}+H_2O\)
0,5------->0,25---->0,25
\(CO_2+CO_3^{2-}+H_2O\rightarrow2HCO_3^-\)
0,15--->0,15-------------->0,3
=> \(\dfrac{1}{2}ddY:\left\{{}\begin{matrix}n_{CO_3^{2-}}=\dfrac{0,25-0,15}{2}=0,05\left(mol\right)\\n_{HCO_3^-}=\dfrac{0,3}{2}=0,15\left(mol\right)\end{matrix}\right.\)
- Phần 1: \(n_{BaCO_3}=n_{HCO_3^-}+n_{CO_3^{2-}}=0,2\left(mol\right)\)
=> a = 0,2.197 = 39,4 (g)
- Phần 2: \(n_{BaCO_3}=n_{CO_3^{2-}}=0,05\left(mol\right)\)
=> b = 0,05.197 = 9,85 (g)
=> a - b = 29,55 (g)
Đúng 2
Bình luận (0)
Dung dịch X chứa 0,2 mol K+ ; 0,4 mol Na+, 0,2 mol OH- và x mol CO32-. Hấp thụ hoàn toàn V lít CO2 (đktc) vào dung dịch X. Làm khô dung dịch X thu 47,4 gam muối khan. Giá trị của V là:
BTĐT: \(n_{CO_3^{2-}}=\dfrac{0,2+0,4-0,2}{2}=0,2\left(mol\right)\)
Gọi \(n_{CO_2}=a\left(mol\right)\)
- TH1: Mới có \(OH^-\) tham gia phản ứng, \(OH^-\) có thể dư
PT: \(CO_2+2OH^-\rightarrow CO_3^{2-}+H_2O\)
a---->2a---------->a
=> \(n_{OH^-\left(dư\right)}=0,2-2a\left(mol\right)\left(a< 0,1\right)\)
=> \(m_{muối}=0,2.39+0,4.23+60a+\left(0,2-2a\right).17+0,2.60=47,4\)
=> \(a=\dfrac{15}{26}\left(KTM\right)\)
=> Loại
- TH2: \(CO_3^{2-}\) đã tham gia phản ứng, \(CO_3^{2-}\) có thể dư
PT: \(CO_2+2OH^-\rightarrow CO_3^{2-}+H_2O\)
0,1<---0,2-------->0,1
=> \(\left\{{}\begin{matrix}n_{CO_2\left(dư\right)}=a-0,1\left(mol\right)\\\sum n_{CO_3^{2-}}=0,1+0,2=0,3\left(mol\right)\end{matrix}\right.\)
\(CO_3^{2-}+CO_2+H_2O\rightarrow2HCO_3^-\)
(a - 0,1)<-(a - 0,1)---------->(2a - 0,2)
=> \(n_{CO_3^{2-}\left(dư\right)}=0,3-\left(a-0,1\right)=0,4-a\left(mol\right)\)
=> 0,1 < a < 0,4
=> \(m_{muối}=0,2.39+0,4.23+60.\left(0,4-a\right)+61.\left(2a-0,2\right)=47,4\)
=> \(a=0,3\left(TM\right)\)
=> \(V=V_{CO_2}=0,3.22,4=6,72\left(l\right)\)
- TH3: \(CO_3^{2-}\) và \(OH^-\) đã hết, \(CO_2\) dư
PT: \(2OH^-+CO_2\rightarrow CO_3^{2-}+H_2O\)
0,1----------------->0,1
=> \(\sum n_{CO_3^{2-}}=0,1+0,2=0,3\left(mol\right)\)
\(CO_3^{2-}+CO_2+H_2O\rightarrow2HCO_3^-\)
0,3-------------------------->0,6
=> \(m_{muối}=0,2.39+0,4.23+0,6.61=53,6\left(g\right)\ne47,4\)
=> Loại
Đúng 1
Bình luận (0)
Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào 100 ml dung dịch gồm K2CO3 0,2M và KOH 1,4 mol/lít, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y.Nếu Cho toàn bộ Y tác dụng với dung dịch Ca(OH)2 (dư), thu được a mol kết tủaNếu Cho toàn bộ Y tác dụng với dung dịch CaCl2 (dư), thu được b mol kết tủa. Tỉ lệ a:b là:
Đọc tiếp
Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào 100 ml dung dịch gồm K2CO3 0,2M và KOH 1,4 mol/lít, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y.
Nếu Cho toàn bộ Y tác dụng với dung dịch Ca(OH)2 (dư), thu được a mol kết tủa
Nếu Cho toàn bộ Y tác dụng với dung dịch CaCl2 (dư), thu được b mol kết tủa.
Tỉ lệ a:b là:
`n_[K_2 CO_3]=0,2.0,1=0,02(mol)`
`n_[CO_2]=[2,24]/[22,4]=0,1(mol)`
`n_[OH^-]=1,4.0,1=0,14(mol)`
`[n_[OH^-]]/[n_[CO_2]]=1,4=>` Tạo muối `HCO_3 ^- ;CO_3 ^[2-]`
`CO_2 + 2KOH -> K_2 CO_3 + H_2 O`
`0,07` `0,14` `0,14` `(mol)`
`H_2 O + CO_2 + K_2 CO_3 -> 2KHCO_3`
`0,03` `0,03` `0,06` `(mol)`
`=>n_[K_2 CO_3]=0,14-0,03+0,02=0,13(mol)`
`K_2 CO_3 + Ca(OH)_2 -> CaCO_3 \downarrow + 2KOH`
`0,13` `0,13` `(mol)`
`KHCO_3 + Ca(OH)_2 -> CaCO_3 \downarrow + KOH + H_2 O`
`0,06` `0,06` `(mol)`
`=>a=0,13+0,06=0,19mol)`
`K_2 CO_3 + CaCl_2 -> CaCO_3 \downarrow + 2KCl`
`0,13` `0,13` `(mol)`
`=>b=0,13(mol)`
Vậy `a:b=0,19:0,13=19/13`
Đúng 2
Bình luận (0)
(Nhớ biện luận số mol nha).
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{K_2CO_3}=0,1.0,2=0,02\left(mol\right)\)
\(n_{KOH}\) là 1,4 mol trên 1 lít.
=> 100ml = 0,1l = \(\dfrac{1}{10}\left(l\right)\)
=> \(n_{KOH}=\dfrac{1}{10}.1,4=0,14\left(mol\right)\)
\(CO_2+K_2CO_3+H_2O\rightarrow2KHCO_3\) (1)
0,02 0,02 0,04
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\) (2)
0,06 0,12 0,06 0,06
\(CO_2+KOH\rightarrow KHCO_3\) (3)
0,02 0,02 0,02
(tự luận số mol hộ e a)
Bổ sung thêm cách biết tạo muối nào ở đây ạ: https://diendan.hocmai.vn/threads/hoa-9-dieu-kien-tao-muoi-trung-hoa-muoi-axit-ca-2-muoi.269780/
gọi x và y lần lượt là số mol của \(CO_2\left(2\right)\) và \(CO_2\left(3\right)\)
có: x + y = 0,08
2x + y = 0,14
=> x = 0,06 và y = 0,02.
Có dd Y gồm: \(KHCO_3;K_2CO_3\)
- Cho Y td Ca(OH)2 dư.
\(Ca\left(OH\right)_2+KHCO_3\rightarrow CaCO_3+H_2O+KOH\) (4)
0,06 0,06
\(Ca\left(OH\right)_2+K_2CO_3\rightarrow CaCO_3+2KOH\) (5)
0,06 0,06
\(n_{KHCO_3\left(4\right)}=n_{KHCO_{3\left(1\right)}}+n_{KHCO_{3\left(3\right)}}=0,04+0,02=0,06\left(mol\right)\)
=> \(a=0,06+0,06=0,12\left(mol\right)\)
- Cho T td với dd CaCl2 dư.
\(KHCO_3+CaCl_2\rightarrow\left(ko.pứ\right)\)
\(K_2CO_3+CaCl_2\rightarrow CaCO_3+2KCl\) (6)
0,06 0,06
=> b = 0,06.
=> \(\dfrac{a}{b}=\dfrac{0,12}{0,06}=2\)
Đúng 0
Bình luận (0)
Câu 2a với c nha.

a) Hòa tan các chất rắn vào dd Ba(OH)2 dư, nếu thấy:
+ Mẫu thử tạo kết tủa trắng: K2CO3
\(K_2CO_3+Ba\left(OH\right)_2\rightarrow BaCO_3\downarrow+2KOH\)
+ Mẫu thử tan: NaNO3
+ Mẫu thử không tan: BaCO3
+ Mẫu thử tạo kết tủa trắng đồng thời có khí thoát ra: (NH4)2SO4
\(\left(NH_4\right)_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+2NH_3\uparrow+2H_2O\)
c) - Hòa tan các chất rắn vào dd H2SO4 dư, nếu thấy:
+ Chất rắn không tan: BaSO4
+ Chất rắn tạo kết tủa trắng đồng thời có khí không màu, không mùi thoát ra: CaCO3
\(CaCO_3+H_2SO_4\rightarrow CaSO_4\downarrow+CO_2\uparrow+H_2O\)
+ Chất rắn tan: NaCl
+ Chất rắn tan, tạo khí không màu, không mùi: Na2CO3
\(Na_2CO_3+H_2SO_4\rightarrow Na_2SO_4+CO_2\uparrow+H_2O\)
Đúng 0
Bình luận (0)
Khử 7,1 gam Fe2O3 bằng CO trong lò nung thu được 4,2 gam fe kim loại. Hiệu suất pứ thu được Fe là
\(n_{Fe}=\dfrac{4,2}{56}=0,075\left(mol\right)\)
PTHH: \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
0,0375<--------0,075
=> \(H\%=\dfrac{0,0375.160}{7,1}.100\%=84,507\%\)
Đúng 2
Bình luận (0)
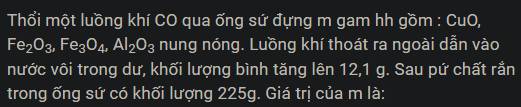
\(m_{tăng}=m_{CO_2}=12,1\left(g\right)\)
=> \(n_{CO_2}=\dfrac{12,1}{44}=0.275\left(mol\right)\)
Bản chất của phản ứng: \(CO+O_{\left(oxit\right)}\xrightarrow[]{t^o}CO_2\)
0,275<----0,275
=> m = 0,275.16 + 225 = 229,4 (g)
Đúng 1
Bình luận (0)
Đọc tiếp