Trong một bình kín dung tích không đổi chứa hỗn hợp A gồm etan và một ankin (đều ở thể khí) có tỉ lệ số mol là 1:1. Thêm oxi vào bình thì được hỗn hợp khí B có tỉ khối so với H2 là 18. Đốt cháy hoàn toàn hỗn hợp B sau đó đưa về 0oC thấy hỗn hợp khí trong bình có tỉ khối so với H2 là 21,4665. Công thức ankin là:
A. C2H2
B. C3H4
C. C4H6
D. C5H8
Đáp án C
Ankin thể khí, do đó số nguyên tử C < 5
Đặt số mol của C2H6: a mol; CnH2n-2: a mol; O2: b mol
Gọi hỗn hợp sau khi đốt là hỗn hợp C ta có:
nB: nC = MC: MB = 21,4665: 18 = 1,2
Chọn: nB = 1,2 mol mB = 18.2.1,2 = 43,2g
Ta có :
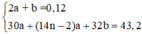
14na – 36a + 32.(2a + b)=43,2g
14na – 36a + 32.1,2 =43,2g
14na – 36a = 4,8 a =
Mà 2a < 12 a < 0,6 hay < 0,6 7n – 18 > 4 n > 3,14
n = 4 ankin là C4H6

