Câu 42 :
n HCl =400.5,475%/36,5 = 0,6(mol)
n CO2 = 2,24/22,4 = 0,1(mol)
m dd Y = 30,5 + 400 - 0,1.44= 426,1(gam)
=> m MCl2 = 426,1.9,58% = 40,82
n MCl2 = 1/2 n HCl = 0,3 mol
=> M MCl2 =M + 35,5.2 = 40,82/0,3 = 136
=> M = 65(Zn)
Đáp án C
Gọi x,y tương ứng là số mol của FeO và Fe2O3
Ta có: 72x + 160y = 31,2 và 127.x/2 + 325.y/2 = 30,725. Giải hệ thu được: x = 0,1;y = 0,15 mol.
Phần 2:
Gọi a, b tương ứng là số mol của HCl và H2SO4. Hỗn hợp muối khan gồm FeCl2, FeCl3, FeSO4 và Fe2(SO4)3.
Ta có: 35,1 = mFe + mCl + mSO4 = 56(0,05 + 0,15) + 35,5a + 96b = 11,2 + 35,5a + 96b
Mặt khác: nCl + 2nSO4 = a + 2b = 2nFeO + 6nFe2O3 = 2.0,05 + 6.0,075 = 0,55
Giải hệ thu được: a = 0,2 và b = 0,175 mol.
=> nHCl (B) = 0,2 (mol)
Câu 41 :
Xem Fe3O4 tạo thành từ hh: Fe2O3 và FeO
=> Hỗn hợp A gồm: FeO, Fe2O3
Gọi x, y là số mol FeO và Fe2O3 trong 1/2 hỗn hợp A. Ta có:
72x + 160y = 31.2/2 = 15.6
127x + 325y = 30.725
=> x = 0.05
y = 0.075
mFe= 0.05 * 56 + 0.075 * 2 * 56 = 11.2(g)
m gốc axit = 35.1 - 11.2 = 23.9 (g)
Đặt :
nCl- = a (mol)
nSO42- = b(mol)
BTĐT:
2nFe+2 + 3nFe+3 = nCl- + 2nSO42-
=> a + 2b = 0.05*2 + 0.075*2*3 = 0.55
36.5a + 96b = 23.9
=> a = 0.2
b = 0.175
=> nHCl = 0.2




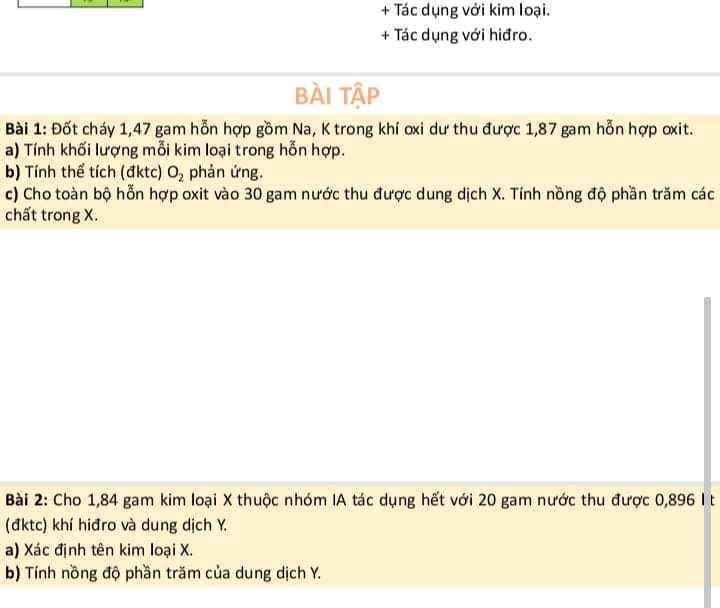



 giúp mình với ạ ;-; . mình đang cần gấp lắm
giúp mình với ạ ;-; . mình đang cần gấp lắm 

