Câu 7. Hai nguyên tử M kết hợp với một nguyên tử O tạo ra phân tử oxit. Trong phân tử, nguyên tử oxi chiếm 25,8% về khối lượng. Công thức của oxit là: *1 pointTùy chọn 4Tùy chọn 1Tùy chọn 3Tùy chọn 2Câu 4. Chọn cặp nguyên tử có cùng tên gọi hóa học: *1 pointChỉ có cặp X, YCặp X, Y và cặp Z, TChỉ có cặp Y, ZChỉ có cặp Z, TCâu 3. Khối lượng tính bằng g của nguyên tử canxi là bao nhiêu? *1 point64,4 x 10^-24 g6,64 x 10^-24 g6,642 x 10^-23 g7,6 x 10^-24 gCâu 8. N trong hợp chất nào sau đây có hóa tr...
Đọc tiếp
Câu 7. Hai nguyên tử M kết hợp với một nguyên tử O tạo ra phân tử oxit. Trong phân tử, nguyên tử oxi chiếm 25,8% về khối lượng. Công thức của oxit là: *
1 point

Tùy chọn 4

Tùy chọn 1

Tùy chọn 3

Tùy chọn 2
Câu 4. Chọn cặp nguyên tử có cùng tên gọi hóa học: *
1 point
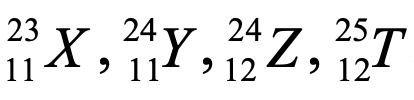
Chỉ có cặp X, Y
Cặp X, Y và cặp Z, T
Chỉ có cặp Y, Z
Chỉ có cặp Z, T
Câu 3. Khối lượng tính bằng g của nguyên tử canxi là bao nhiêu? *
1 point
64,4 x 10^-24 g
6,64 x 10^-24 g
6,642 x 10^-23 g
7,6 x 10^-24 g
Câu 8. N trong hợp chất nào sau đây có hóa trị 4? *
1 point

Tùy chọn 2

Tùy chọn 4

Tùy chọn 3

Tùy chọn 1
Câu 1. Mệnh đề nào sau đây KHÔNG đúng: *
1 point
Số khối của nguyên tử bằng số êlêctron cộng với số nơtron
Khối lượng của hạt nhân lớn hơn khối lượng của nguyên tử
Chỉ có hạt nhân nguyên tử ôxi mới có 8 prôton
Prôton và nơtron có cùng khối lượng
Câu 10. Kim loại M tạo ra oxit M2O3 có phân tử khối của oxit là 160. Nguyên tử khối của M là: *
1 point
27
56
64
24
Câu 9. Cho hợp chất của X là XO và Y là Na2Y. Công thức hợp chất tạo bởi X và Y là: *
1 point

Tùy chọn 4

Tùy chọn 2

Tùy chọn 3

Tùy chọn 1
Câu 2. Một hợp chất mà phân tử gồm 2 nguyên tử của nguyên tố X liên kết với 1 nguyên tử ôxi và có phân tử khối là 62 đvC. X là nguyên tố nào sau đây? *
1 point
Na
Ca
Mg
K
Câu 6. Nguyên tố X có nguyên tử khối (NTK) bằng 3,5 lần NTK của oxi, nguyên tử Y nhẹ bằng 1/4 nguyên tử X. Vậy X, Y lần lượt là 2 nguyên tố nào cho dưới đây? *
1 point
Fe và N
Na và Cu
K và N
Ca và N
Câu 5. Nguyên tử nào trong các nguyên tử sau đây có 20 proton, 20 electron, 18 nơtron? *
1 point

Tùy chọn 2

Tùy chọn 4

Tùy chọn 3

Tùy chọn 1




