cân bằng bằng phương pháp thăng bằng electron
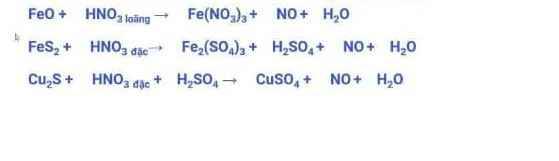
cân bằng bằng phương pháp thăng bằng electron

| $Fe^{+2} \to Fe^{+3} + 1e$ | x3 |
| $N^{+5} + 3e \to N^{+2}$ | x1 |
$3FeO + 10HNO_3 \to 3Fe(NO_3)_3 + NO + 5H_2O$
| $FeS_2 \to Fe^{+3} + 2S^{+6} + 15e$ | x2 |
| $N^{+5} + 3e \to N^{+2}$ | x10 |
$2FeS_2 + 10HNO_3 \to Fe_2(SO_4)_3 + H_2SO_4 + 10NO + 4H_2O$
| $Cu_2S \to 2Cu^{+2} + S^{+6} + 10e$ | x3 |
| $N^{+5} + 3e \to N^{+2}$ | x10 |
$3Cu_2S + 10HNO_3 + 3H_2SO_4 \to 6CuSO_4 + 10NO + 8H_2O$
K2SO3 + KMnO4 + KHSO4-----> K2SO4 + MnSO4+H2O
cân bằng với phương pháp đại số giúp mình nhé
\(aK_2SO_3+bKMnO_4+cKHSO_4\rightarrow dK_2SO_4+eMnSO_4+fH_2O\)
Bảo toàn K: 2a + b + c = 2d (1)
Bảo toàn S: a + c = d + e (2)
Bảo toàn Mn: b = e (3)
Bảo toàn H: c = 2f (4)
Bảo toàn O: 3a + 4b + 4c = 4d + 4e + f (5)
(2) => a + c - b = d (**)
(5) => 3a + 4b + 4c - 4b - 0,5c = 4d
=> 3a + 3,5c = 4d (***)
(1)(**)(***) => \(\left\{{}\begin{matrix}a=\dfrac{5}{9}d\\b=\dfrac{2}{9}d\\c=\dfrac{2}{3}d\end{matrix}\right.\) => \(\left\{{}\begin{matrix}e=\dfrac{2}{9}d\\f=\dfrac{1}{3}d\end{matrix}\right.\)
Chọn d = 9 => \(\left\{{}\begin{matrix}a=5\\b=2\\c=6\\e=2;f=3\end{matrix}\right.\)
Vậy \(5K_2SO_3+2KMnO_4+6KHSO_4\rightarrow9K_2SO_4+2MnSO_4+3H_2O\)
Cho hỗn hợp ZN,Al tác dụng với dung dịch H2SO4 8M đặc thu được 50,3g muối tính %M ZN
bn check lại đề xem thiếu dữ kiện gì không nhé :)
1 tăng nhiêtj độ
2 tăng số chất tham gia pứ
3 giảm chất sản phẩm
Giúp câu 13 để ôn tập vs ạ
13)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
=> \(n_{H_2SO_4}=0,2\left(mol\right)\)
=> \(V_{dd.H_2SO_4}=\dfrac{0,2}{0,2}=1\left(l\right)=1000\left(ml\right)\)
Giúp mình với mng ơi 
Ta có: 64nCu+27nAl=5,9 (1).
Số mol khí SO2 tạo thành là 4,48/22,4=0,2 (mol).
BTe: 2nCu+3nAl=2.0,2=0,4 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra nCu=0,05 (mol) và nAl=0,1 (mol).
Khối lượng muối sunfat gồm CuSO4 (0,05 mol) và Al2(SO4)3 (0,05 mol) là 0,05.160+0,05.102=13,1 (g).

B) Sử dụng chất chỉ thị nào?Tại sao phép định lượng glucose, phải cho chỉ thị vài khi dung dịch có màu vàng rơm (vàng nhạt)?
Chủ đề là định lượng glucose ;-;;;
a) nH2 = 0,195 (mol)
PTHH : \(Mg+2HCl-->MgCl_2+H_2\)
\(2Al+6HCl-->2AlCl_3+3H_2\)
Đặt \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Al}=y\end{matrix}\right.\) => \(\left\{{}\begin{matrix}24x+27y=3,87\\x+\dfrac{3}{2}y=0,195\end{matrix}\right.\) => \(\left\{{}\begin{matrix}x=0,06\\y=0,09\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Mg}=1,44\left(g\right)\\m_{Al}=2,43\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Mg}=37,2\%\\\%m_{Al}=62,8\%\end{matrix}\right.\)
b) nHCl pứ = 2nH2 = 0,39 (mol)
=> nHCl dư = 0,39.5/100 = 0,0195 (mol)
BT Mg : nMgCl2 = nMg = 0,06 (mol)
BT Al : nAlCl3 = nAl = 0,09 (mol)
=> \(C_{M\left(MgCl2\right)}=\dfrac{0,06}{0,5}=0,12\left(M\right)\)
\(C_{M\left(AlCl_3\right)}=\dfrac{0,09}{0,5}=0,18\left(M\right)\)
\(C_{M\left(HCl\right)}=\dfrac{0,0195}{0,5}=0,039\left(M\right)\)