GIÚP EM VỚI Ạ
Câu 5 : Trong phản ứng hoá học, nguyên tử Clo nhận electron hình thành được ion
A.Cl+. B.Cl2+. C.Cl . D.Cl .
GIÚP EM VỚI Ạ
Câu 5 : Trong phản ứng hoá học, nguyên tử Clo nhận electron hình thành được ion
A.Cl+. B.Cl2+. C.Cl . D.Cl .
Al + Fe3+
sự khác nhau giữa ion đa nguyên tử và ion đơn nguyên tử là gì
Giải thích sự tạo thành liên kết ion trong hợp chất Na2S, MgCl2 từ các đơn chất.
_
_
__
_
Giúp em với ạ
cho 12MG 19K 8O 17Cl viết quá trình hình thành liên kết ion trong phân tử a MgO b KCl
Giúp em với Tại sao nguyên tu lai có xu huong nhường hoặc nhận electron ?
Sắp xếp các phân tử sau theo chiều độ phân cực giảm dần:
K2O, N2, H2S, HCl
(ZK = 19; ZN = 7; ZS = 16; ZCl = 17)
Câu 1: Nguyên tử X có cấu hình electron 1s22s22p63s23p3. X thuộc nhóm
A. IIIA B.IIIB
C.VA D.VB
Câu 2: Trong cùng một nhóm A, theo chiều tăng của điệm tích hạt nhân, độ âm điện biến đổi như thế nào?
A. Giảm xuống.
B. Tăng lên.
C. Biến đổi không theo quy luật.
D. Không thay đổi.
Câu 3: Khối lượng của nguyên tử được coi như bằng tổng khối lượng của
A. electron và proton
B. electron và notron
C. notron và proton
D. chỉ nguyên proton
Câu 4:
Ở trạng thái cơ bản các electron lần lượt chiếm các mức năng lượng từ thấp đến cao. Thứ tự sắp xếp các phân lớp theo chiều tăng của năng lượng là
A. 1s 2s 2p 3s 3p 3d 4s 4p 5s…
B. 1s 2s 2p 3s 3p 4s 3d 4p 5s…
C. 1s 2s 2p 3s 3p 3d 4p 4s 5s…
D. 1s 2s 3s 4s 5s 2p 3p 4p 3d …
Câu 5: Số electron lớp ngoài cùng của nguyên tử X có cấu hình 1s22s22p63s23p6 là bao nhiêu?
A.2
B.6
C.8
D.3
Hộ mình với nhaaa
Câu 1: Nguyên tử X có cấu hình electron 1s22s22p63s23p3. X thuộc nhóm
A. IIIA B.IIIB
C.VA D.VB
Do có lớp ngoài cùng là 3s23p3
Câu 2: Trong cùng một nhóm A, theo chiều tăng của điệm tích hạt nhân, độ âm điện biến đổi như thế nào?
A. Giảm xuống.
B. Tăng lên.
C. Biến đổi không theo quy luật.
D. Không thay đổi.
Câu 3: Khối lượng của nguyên tử được coi như bằng tổng khối lượng của
A. electron và proton
B. electron và notron
C. notron và proton
D. chỉ nguyên proton
Do khối lượng của electron không đáng kể nên khối lượng của nguyên tử được xem như bằng khối lượng hạt nhân
Câu 4:
Ở trạng thái cơ bản các electron lần lượt chiếm các mức năng lượng từ thấp đến cao. Thứ tự sắp xếp các phân lớp theo chiều tăng của năng lượng là
A. 1s 2s 2p 3s 3p 3d 4s 4p 5s…
B. 1s 2s 2p 3s 3p 4s 3d 4p 5s…
C. 1s 2s 2p 3s 3p 3d 4p 4s 5s…
D. 1s 2s 3s 4s 5s 2p 3p 4p 3d …
Câu 5: Số electron lớp ngoài cùng của nguyên tử X có cấu hình 1s22s22p63s23p6 là bao nhiêu?
A.2
B.6
C.8
D.3
Lớp ngoài cùng 3s23p6
X,Y,Z có tổng số điện tích hạt nhân là 16 . Hiệu điện tích hạt nhân giữa X và Y là 1 . Số e trong ion [YX3]- là 32 , xác định X ,Y,Z và ion [YX3]-
Gọi số e trong mỗi nguyên tử X,Y,Z lần lượt là x,y,z. Theo đề bài ta có hệ phương trình đại số:
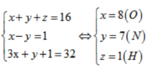
Tổng số các hạt trong nguyên tử (X) là 48. trong đó số hạt mang điện dương bằng số hạt không mang điện.
a. Xác định số proton, số electron, số notron trong (X)
b. Tính số khối của (X)
c. viết cấu hình electron nguyên tử (X)