Đề cương ôn tập : CTCT-Metan-Etilen-Axetilen
Nội dung lý thuyết
Các phiên bản khácĐỀ CƯƠNG ÔN TẬP:
CẤU TẠO CHẤT HỮU CƠ-METAN-ETILEN-AXETILEN
I. KIẾN THỨC CẦN NHỚ
1. Một số khái niệm về hợp chất hữu cơ.
- Những hợp chất nào được gọi là hợp chất hữu cơ?
- Phân loại hợp chất hữu cơ?
- Hóa trị của các nguyên tố trong hợp chất hữu cơ?
- Công thức cấu tạo của hợp chất hữu cơ là gì? Cách viết CTCT của một hợp chất hữu cơ?
2. Metan-Etilen-Axetilen
| Metan | Etilen | Axetilen |
Tính chất vật lí | Khí không màu, không mùi, ít tan trong nước | Khí không màu, không mùi, ít tan trong nước | Khí không màu, không mùi,ít tan trong nước
|
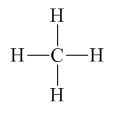
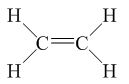
Công thức cấu tạo |
CH4 |
CH2=CH2 |
CH≡CH |
Tính chất hóa học Phản ứng đốt cháy | Phản ứng tỏa nhiều nhiệt. CH4 + 2O2 \(\underrightarrow{t^o}\) 2H2O + CO2 | Phản ứng tỏa nhiều nhiệt. C2H4 + 3O2 \(\underrightarrow{t^o}\) 2H2O + 2CO2 | Phản ứng tỏa nhiều nhiệt. 2C2H2 + 5O2 \(\underrightarrow{t^o}\) 2H2O + 4CO2 |
Phản ứng thế | Phản ứng đặc trưng của metan là phản ứng thế. CH4 + Cl2 \(\underrightarrow{ás}\) CH3Cl + HCl
|
|
|
Phản ứng cộng |
| CH2=CH2+H2 \(\underrightarrow{t^o,Ni}\) CH3-CH3 CH2=CH2+Br2 → BrCH2-CH2Br | CH≡CH+H2\(\underrightarrow{t^o,Pd/PbCO_3}\)CH2=CH2 CH≡CH+2H2\(\underrightarrow{t^o,Ni}\)CH3-CH3
CH≡CH+2Br2 →Br2CH-CHBr2 |
Phản ứng trùng hợp |
| n(CH2=CH2)\(\underrightarrow{t^o,p,xt}\) –(CH2-CH2)n |
|
Điều chế | Nguồn từ dầu mỏ, khí thiên nhiên. | Nguồn từ dầu mỏ, khí thiên nhiên. | Nguồn từ dầu mỏ, khí thiên nhiên. CaC2+H2O→ Ca(OH)2+C2H2 2CH4 \(\underrightarrow{1500^oC}\) C2H2 + 3H2 |
Ứng dụng | -Nhiên liệu -Nguyên liệu của phản ứng điều chế khí hiđro, bột than,… | -Kích thích quả mau chín. -Nhiên liệu. -Nguyên liệu để sản xuất PE, cồn, axit axetic. | -Đèn xì axetilen. -Nguyên liệu sản xuất PVC, cao su,… |
II.BÀI TẬP
PHẦN 1. TRẮC NGHIỆM
Câu 1. Cho các chất sau: CH4, CH3Cl, CO, CO2, CH3COOH, H2CO3,C2H5ONa, NaHCO3, BaCO3, C2H4, C2H6, C6H6. Trong dãy đó có bao nhiêu hợp chất hữu cơ?
A.5 B.6 C.8 D.10
Câu 2. Dãy các chất nào sau đây đều là hiđrocacbon?
A.C2H4, CH4, C2H5Cl B.CH4, C2H2, CH3Cl
C.C2H6, CH4, C2H4 D.CH4O, C3H6, C2H2
Câu 3. Công thức cấu tạo của hợp chất cho biết điều gì?
A.Trật tự liên kết giữa các nguyên tử trong phân tử.
B.Thành phần phân tử.
C.Thành phần phân tử và sự tham gia liên kết với các hợp chất khác.
D.Thành phần phân tử và trật tự liên kết giữa các nguyên tử trong phân tử.
Câu 4. Có mấy loại liên kết giữa 2 nguyên tử cacbon?
A.1 B.2 C.3 D.4.
Câu 5. Các công thức cấu tạo nào biểu diễn chất khác so với 3 công thức còn lại ?
A. CH3-O-CH3
B. CH3-CH2-OH
C. HO-CH2-CH3
D. CH3-CH2-O-H
Câu 6. Chọn câu đúng trong các câu sau:
A. Metan có nhiều trong khí quyển.
B. Metan có nhiều trong mỏ khí, mỏ dầu, mỏ than.
C. Metan có nhiều trong nước biển.
D. Metan có nhiều trong các hang động.
Câu 7. Phản ứng đặc trưng của metan là
A. phản ứng cháy. B. phản ứng cộng.
C. phản ứng thế. D. phản ứng trùng hợp.
Câu 8. Trong thí nghiệm điều chế khí metan, khí metan có thể thu được bằng phương pháp đẩy nước vì
A.khí metan nhẹ hơn không khí.
B.metan tồn tại ở trạng thái khí ở nhiệt độ thường.
C.khí metan ít tan trong nước.
D.khí metan nhẹ hơn nước.
Câu 9. Metan có phản ứng với chất nào sau đây?
A.Cl2 B.CO C.H2 D.CO2
Câu 10. Cho khí metan tác dụng với khí clo theo tỉ lệ mol 1:1. Sản phẩm tạo thành là
A.CH3Cl B.CH2Cl2 C.CHCl3 D.CCl4
Câu 11. Số liên kết đơn và liên kết đôi trong phân tử khí etilen là
A.bốn liên kết đơn và hai liên kết đôi.
B.ba liên kết đơn và hai liên kết đôi.
C.bốn liên kết đơn và một liên kết đôi.
D.hai liên kết đơn và hai liên kết đôi.
Câu 12. Loại bỏ khí etilen lẫn trong metan người ta sử dụng phương pháp hóa học nào?
A. Đốt cháy hỗn hợp trong không khí
B. Dẫn hỗn hợp khí đi qua dung dịch brom dư
C. Dẫn hỗn hợp khí đi qua dung dịch muối ăn
D. Dẫn hỗn hợp khí đi quan nước
Câu 13. Một hiđrocacbon X khi đốt cháy tuân theo phương trình hóa học sau:
X + 3O2 \(\underrightarrow{t^o}\) 2CO2 + 2H2O
Hiđrocacbon X là
A. etilen B. axetilen C.metan D.etan
Câu 14. Dãy các chất nào sau đây đều làm mất màu dung dịch nước brom?
A.CH4, C2H6 B.C2H4, C2H6
C.CH4, C2H4 D.C2H4, C2H2
Câu 15. Trong điều kiện thích hợp, liên kết kém bền trong các phân tử etilen có thể bứt dứt ra. Khi đó, các phân tử etilen kết hợp với nhau tạo thành phân tử có kích thước và khối lượng rất lớn. Những phân tử đó có tên gọi là
A.etan B.polietan C.polietilen D.etilen
Câu 16. Axetilen có tính chất vật lý
A. là chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
B. là chất khí không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. là chất khí không màu, không mùi, tan trong nước, nhẹ hơn không khí .
D. là chất khí không màu, mùi hắc, ít tan trong nước, nặng hơn không khí.
Câu 17. Liên kết C≡C trong phân tử axetilen có đặc điểm
A. một liên kết kém bền dễ đứt ra trong các phản ứng hóa học.
B. hai liên kết kém bền nhưng chỉ có một liên kết bị đứt ra trong phản ứng hóa học.
C. hai liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
D. ba liên kết kém bền dễ đứt lần lượt trong các phản ứng hóa học.
Câu 18. Một hiđrocacbon ở thể khí là nhiên liệu của đèn xì thường dùng để hàn cắt kim loại. Hiđrocacbon đó là
A. metan B. etilen C.axetilen D. etan
Câu 19. Khi đốt khí axetilen, số mol CO2 và H2O được tạo thành theo tỉ lệ là
A. 2 : 1 B. 1 : 2 C. 1 : 3 D. 1 : 1.
Câu 20. Khí axetilen không có tính chất hóa học nào sau đây ?
A. Phản ứng cộng với dung dịch brom.
B. Phản ứng cháy với oxi.
C. Phản ứng cộng với hiđro.
D. Phản ứng thế với clo ngoài ánh sáng.
Câu 21. Phương pháp hiện đại để điều chế axetilen hiện nay là
A. nhiệt phân etilen ở nhiệt độ cao.
B. nhiệt phân benzen ở nhiệt độ cao.
C. nhiệt phân canxi cacbua ở nhiệt độ cao.
D. nhiệt phân metan ở nhiệt độ cao.
Câu 22. 1 mol hiđrocacbon X làm mất màu vừa đủ 2 mol brom trong dung dịch. Hiđrocacbon X là
A. CH4 B. C2H4 C. C2H2 D. C6H6
Câu 23. Đốt cháy hoàn toàn 0,224 lít khí axetilen thì cần bao nhiêu lít không khí (các khí đo ở đktc, biết rằng oxi chiếm 20% thể tích không khí) ?
A. 3 lít B. 2,8 lít C. 2,4 lít D. 1,2 lít.
Câu 24. Trong điều kiện thích hợp 1 mol khí axetilen tác dụng hoàn toàn với 2 mol khí hiđro, thu được chất khí là
A. C2H4 B. C2H6 C. C3H4 D. C3H6.
Câu 25. Để phân biệt các chất khí sau: CH4, C2H2, CO2 người ta dùng hóa chất nào sau đây?
A.Dung dịch Brom, Ca(OH)2 B.Dung dịch Brom
C.Brom khan D.AgNO3/NH3
PHẦN 2. TỰ LUẬN
Bài 1. Viết công thức cấu tạo của các chất có công thức phân tử như sau:
CH3Cl, CH4O, C2H6, C2H6O, C2H5Cl, C3H8, C3H8O.
Bài 2. Lập PTHH giữa các chất sau
a. CH4 và Cl2 (tỉ lệ mol 1:1).
b. C2H4 và H2 (điều kiện: toC, p, Ni).
c. C2H4 và Br2 .
d. C2H2 và H2 (Tỉ lệ mol 1:1, điều kiện: toC, Pd/PbCO3).
e. C2H2 và O2 (điều kiện: toC).
Bài 3. Đốt cháy hoàn toàn 4,5g hợp chất hữu cơ A .Biết A chứa C,H,O và thu được 9,9g khí CO2 và 5,4g H2O. Lập công thức phân tử của A, biết phân tử khối A là 60.
Bài 4. Khi phân tích một hiđrocacbon, người ta thấy hiđro chiếm 25% khối lượng. Xác định công thức phân tử của hiđrocacbon, biết phân tử khối của hiđrocacbon bằng 16.
Bài 5. Đốt cháy 6,4 gam chất hữu cơ A thu được 8,8 g CO2 và 7,2 g H2O.Biết MA = 32g/mol. Tìm công thức phân tử A.
Bài 6. Đốt cháy V lít khí metan (đktc) , thu được 1,8g hơi nước.
a. Hãy tính V và thể tích không khí (đktc) cần dùng để đốt cháy hoàn toàn lượng khí metan trên. (không khí chứa 20% khí O2, 80% khí N2).
b. Dẫn toàn bộ sản phẩm của phản ứng đốt cháy đi qua nước vôi trong dư, tính khối lượng kết tủa thu được.
Bài 7. Cho 5,6 lít (đktc) hỗn hợp CH4 và C2H4 đi qua nước brom dư thấy có 4g brom tham gia phản ứng.
a. Viết phương trình phản ứng xảy ra.
b. Tính thành phần phần trăm thể tích mỗi khí trong hỗn hợp ban đầu.
c. Tính thể tích O2 (đktc) cần dùng để đốt cháy hoàn toàn hỗn hợp khí ban đầu.
Bài 8. Đốt cháy hoàn toàn 1,68 lít hỗn hợp gồm 2 khí CH4 và C2H2. Dẫn toàn bộ khí sinh ra qua bình đựng dd Ba(OH)2 dư thấy trong bình có 19,7g kết tủa.
a. Viết PTHH của các phản ứng đã xảy ra.
b. Tính thành phần % thể tích mỗi khí trong hỗn hợp ban đầu.
c. Tính thể tích không khí (đktc) cần để đốt cháy hoàn toàn lượng khí tban đầu.
Bài 9. Cho 11,2 lít hỗn hợp metan và axetilen (đo ở đktc) đi qua dung dịch brom dư thấy có 8 gam Brom tham gia phản ứng :
a. Viết các phương trình phản ứng xảy ra.
b. Tính khối lượng C2H2Br4 thu được sau phản ứng.
c. Tính phần trăm về thể tích của mỗi khí trong hỗn hợp đầu.
Bài 10. Cho 0,56 lít hỗn hợp khí gồm C2H4, C2H2 (đktc) tác dụng hết với dung dịch Br2 dư, lượng Br2 đã tham gia phản ứng là 5,6 gam.
a. Hãy viết phương trình hóa học của các phản ứng đã xảy ra.
b. Tính thể tích mỗi khí có trong hỗn hợp ban đầu.
c. Tính thể tích khí oxi (đktc) cần dung để đốt cháy hoàn toàn lượng khí ban đầu.