Những nguyên tử nào dưới đây thuộc cùng một nguyên tố hóa học?
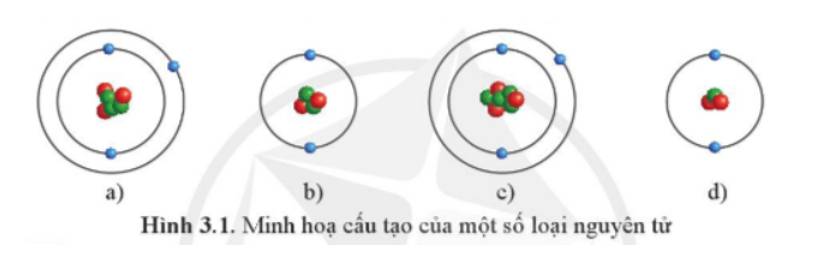
Những nguyên tử nào dưới đây thuộc cùng một nguyên tố hóa học?

Nguyên tử lithium (Li) có 3 proton trong hạt nhân. Khi Li tác dụng với khí chlorine (Cl2) sẽ thu được muối lithium chloride (LiCl), trong đó, Li tồn tại ở dạng ion Li+. Ion Li+ có bao nhiêu proton trong hạt nhân?
- Nguyên tử Li và ion Li+ đều thuộc cùng 1 nguyên tố hóa học là Li
- Li+ là nguyên tử Li sau khi mất đi 1 electron. Do vậy Li+ sẽ có 3 proton và 2 electron
=> Trong hạt nhân Li và Li+ đều có cùng số hạt proton là 3.
Trả lời bởi Hà Quang MinhPhân tử S8 có 128 electron, hỏi số hiệu nguyên tử của lưu huỳnh (S) là bao nhiêu?
- Phân tử S8 nghĩa là có 8 nguyên tử S
=> 1 nguyên tử S có 128 : 8 = 16 electron
- Nguyên tử trung hòa về điện có số hạt proton = số hạt electron
=> Nguyên tử S có 16 proton
- Mà số proton trong một hạt nhân nguyên tử được gọi là số hiệu nguyên tử
=> Nguyên tử S có số hiệu nguyên tử là 16
Trả lời bởi Hà Quang MinhMột nguyên tử có Z hạt proton, Z hạt electron và N hạt neutron. Tính khối lượng (gần đúng theo amu) và số khối của nguyên tử này. Nhận xét về kết quả thu được.
Ta có:
+ Khối lượng nguyên tử = số proton + số neutron + số electron. 0,00055 = Z + N + 0,00055.Z ≈ Z + N
+ Số khối nguyên tử = số proton + số neutron = Z + N
Như vật khối lượng (gần đúng, theo amu) và số khối của nguyên tử có thể coi là bằng nhau.
Trả lời bởi Hà Quang MinhMột loại nguyên tử lithium có 3 proton và 4 neutron. Viết kí hiệu nguyên tử của lithium đó.
- Nguyên tử C có 6 proton, 6 neutron
=> Số hiệu nguyên tử Z = 6, số khối A = số proton + số neutron = 6 + 6 = 12
- Kí hiệu nguyên tử: \({}_{11}^{23}X\)
=> Số proton = Z = 11, số neutron = A – số proton = 23 – 11 = 12
Trả lời bởi Hà Quang MinhHoàn thành bảng sau:

Nguyên tử | Số p | Số n | Kí hiệu nguyên tử |
C | 6 | 6 | \({}_6^{12}C\) |
X | 11 | 12 | \({}_{11}^{23}X\) |
Cho các nguyên tử sau:
\({}_2^5X\), \({}_3^7Y\), \({}_4^9Z\), \({}_5^{11}M\), \({}_5^{12}T\)
Những nguyên tử nào là đồng vị của nhau?
- Trong các nguyên tử: \({}_2^5X\), \({}_3^7Y\), \({}_4^9Z\), \({}_5^{11}M\), \({}_5^{12}T\). Chỉ có nguyên tử M và T là có số hiệu nguyên tử (số proton) bằng nhau.
=> Nguyên tử M và T là đồng vị của nhau.
Trả lời bởi Hà Quang MinhNguyên tố oxygen có 17 đồng vị, bắt đầu từ \({}_8^{12}O\), kết thúc là \({}_8^{28}O\). Các đồng vị oxygen có tỉ lệ giữa số hạt neutron (N) và số hiệu nguyên tử thỏa mãn \(1 \leqslant \frac{N}{Z} \leqslant 1,25\)thì bền vững. Hỏi trong tự nhiên thường gặp đồng vị nào của oxygen?
Ta có: Nguyên tử oxygen có số hiệu nguyên tử Z = 8
Mà số hiệu nguyên tử thỏa mãn \(1 \leqslant \frac{N}{Z} \leqslant 1,25\) thì bền vững
Thay Z vào bất phương trình \(1 \leqslant \frac{N}{Z} \leqslant 1,25\) ta được:
\(1 \leqslant \frac{N}{8} \leqslant 1,25\)
=> \(8 \leqslant N \leqslant 10\)
=> \(8 + Z \leqslant N + Z \leqslant 10 + Z\)
=> \(16 \leqslant A \leqslant 18\)
Vậy các đồng vị thường gặp của oxygen là: \({}_8^{16}O\), \({}_8^{17}O\), \({}_8^{18}O\).
Trả lời bởi Hà Quang MinhEm hãy tìm hiểu đồng vị nào của oxygen chiếm tỉ lệ lớn nhất trong tự nhiên.
Trong tự nhiên:
+ Đồng vị \({}_8^{16}O\) chiếm 99,757%
+ Đồng vị \({}_8^{17}O\) chiếm 0,039%
+ Đồng vị \({}_8^{18}O\) chiếm 0,204%
=> Đồng vị \({}_8^{16}O\) của oxygen chiếm tỉ lệ lớn nhất trong tự nhiên
Trả lời bởi Hà Quang MinhTrong tự nhiên, argon có các đồng vị \({}^{40}{\text{Ar}}\),\(^{38}{\text{Ar}}\), \({}^{36}{\text{Ar}}\)chiếm tương ứng khoảng 99,604%; 0,063% và 0,333% số nguyên tử. Tính nguyên tử khối trung bình của Ar.
Ta có: \({}^{40}{\text{Ar}}\) chiếm 99,604%; \(^{38}{\text{Ar}}\) chiếm 0,063%; \({}^{36}{\text{Ar}}\)chiếm 0,333%
=> \({M_{{\text{Ar}}}} = \frac{{99,694.40 + 0,063.38 + 0,333.36}}{{100}} = 40,02\)
Vậy nguyên tử khối trung bình của Ar là 40,02.
Trả lời bởi Hà Quang Minh
Các nguyên tử mà hạt nhân có cùng số proton thuộc cùng một nguyên tố hóa học.
Nguyên tử ở hình a) và c) thuộc cùng một nguyên tố hóa học vì cùng có 3 proton (hạt màu đỏ).
Nguyên tử ở hình b) và d) thuộc cùng một nguyên tố hóa học vì cùng có 2 proton (hạt màu đỏ).
Trả lời bởi Hà Quang Minh