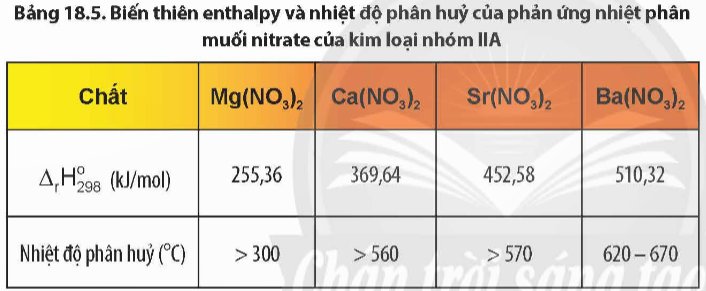
Quan sát Bảng 18.5, nhận xét xu hướng biến đổi độ bền nhiệt của muối nitrate. Từ đó rút ra mối quan hệ giữa độ bền nhiệt và giá trị biến thiên enthalpy của phản ứng nhiệt phân muối nitrate kim loại nhóm IIA.
Quan sát Bảng 18.5, nhận xét xu hướng biến đổi độ bền nhiệt của muối nitrate. Từ đó rút ra mối quan hệ giữa độ bền nhiệt và giá trị biến thiên enthalpy của phản ứng nhiệt phân muối nitrate kim loại nhóm IIA.

Hoàn thành phương trình hoá học của các phản ứng sau:
a) MgCO3 \(\underrightarrow{t^o}\)
b) Ba(NO3)2 \(\underrightarrow{t^o}\)
a: \(MgCO_3\rightarrow^{t^0}MgO+CO_2\)
b: \(Ba\left(NO_3\right)_2\rightarrow^{t^0}Ba\left(NO_2\right)_2+O_2\)
Trả lời bởi Nguyễn Lê Phước ThịnhDựa vào Bảng 18.3, nhận xét sự biến đổi độ tan từ Be(OH)2 đến Ba(OH)2.

Quan sát Bảng 18.4, nhận xét về xu hướng biến đổi độ bền nhiệt của muối carbonate từ MgCO3 đến BaCO3.
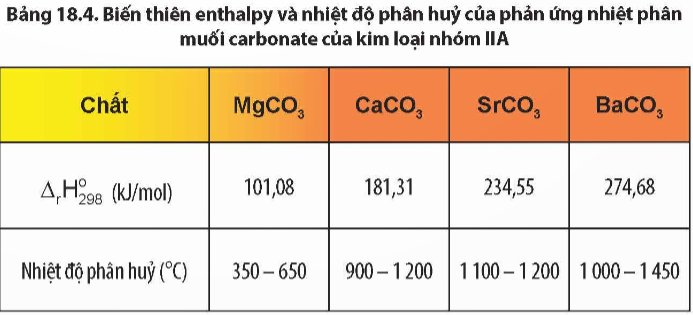
Độ bền nhiệt của muối carbonate của kim loại nhóm IIA có xu hướng tăng dần từ muối của MgCO3 đến muối của BaCO3.
Trả lời bởi datcoderHoàn thành phương trình hoá học của các phản ứng sau:
a) Ca + H2O →
b) Ba + H2O →
a: \(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\uparrow\)
b: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\)
Trả lời bởi Nguyễn Lê Phước ThịnhHoàn thành phương trình hoá học của các phản ứng sau:
a) Be + O2 →
b)Ca + O2→
c) Ba + O2 →
Dựa vào Bảng 18.2, hãy nhận xét sự thay đổi nhiệt độ nóng chảy và khối lượng riêng của kim loại nhóm IIA. Giải thích.
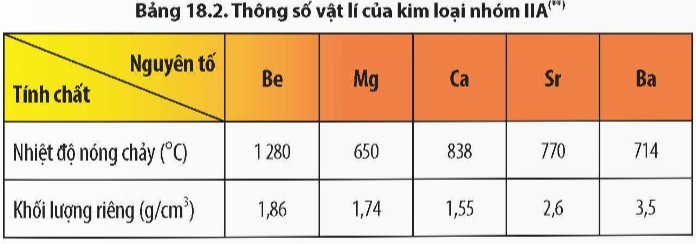
Sự biến đổi nhiệt độ nóng chảy của kim loại nhóm IIA không theo quy luật do cấu trúc mạng tinh thể của kim loại nhóm IIA khác nhau:
+ Beryllium và magnesium có cấu trúc lục phương chặt khít;
+ Calcium và strontium có cấu trúc lập phương tâm mặt;
+ Barium có cấu trúc lập phương tâm khối.
Trả lời bởi datcoderKim loại nhóm IIA và hợp chất của chúng có nhiều ứng dụng trong đời sống, sản xuất.
Kim loại nhóm IIA và hợp chất của chúng có những tính chất gì?
- Kim loại nhóm IIA:
+ Tính chất vật lí: Nhiệt độ nóng chảy, khối lượng riêng và độ cứng của kim loại nhóm IIA cao hơn so với kim loại nhóm IA cùng chu kì. Kim loại nhóm IIA là những kim loại nhẹ (D < 5 g/cm3).
+ Tính chất hóa học: Kim loại nhóm IIA có tính khử mạnh, tính khử tăng dần từ Be đến Ba.
\({\rm{M}} \to {{\rm{M}}^{2 + }} + 2{\mathop{\rm e}\nolimits} \)
- Hợp chất của kim loại nhóm IIA:
+ Muối carbonate: Muối carbonate tác dụng với dung dịch acid loãng, phản ứng với H2O khi có mặt CO2. Dưới tác dụng của nhiệt, muối carbonate của kim loại nhóm IIA bị phân huỷ tạo thành oxide.
+ Muối nitrate: Khi đun nóng, muối nitrate của kim loại nhóm IIA phân huỷ thành oxide.
+ Độ bền nhiệt của muối carbonate, muối nitrate của kim loại nhóm IIA có xu hướng tăng dần từ muối của Mg2+ đến muối của Ba2+.
Trả lời bởi datcoderDự đoán tính chất hoá học đặc trưng của kim loại nhóm IIA và so sánh với kim loại nhóm IA.
Kim loại nhóm IIA có tính khử mạnh nhưng yếu hơn kim loại nhóm IA.
Trả lời bởi datcoderDự đoán khả năng phản ứng của muối carbonate kim loại nhóm IIA với dung dịch acid loãng.
Muối carbonate kim loại nhóm IIA với dung dịch acid loãng giải phóng khí carbon dioxide.
Trả lời bởi datcoder
- Độ bền nhiệt của muối nitrate của kim loại nhóm IIA có xu hướng tăng dần từ muối của Mg(NO3)2 đến muối của Ba(NO3)2.
- Độ bền nhiệt của muối nitrate càng lớn, biến thiên enthalpy của phản ứng nhiệt phân muối nitrate càng lớn.
Trả lời bởi datcoder