Trong các phản ứng hoá học, có một loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu. Do vậy, phản ứng xảy ra không hoàn toàn và thường có hiệu suất không cao. Phản ứng tổng hợp ammonia từ nitrogen và hydrogen thuộc loại phản ứng này. Các phản ứng này được gọi là phản ứng gì? Để tăng hiệu suất của chúng, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ,... như thế nào?
Bài 1. Khái niệm về cân bằng hóa học
H24
Trong các phản ứng hoá học, có một loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu. Do vậy, phản ứng xảy ra không hoàn toàn và thường có hiệu suất không cao. Phản ứng tổng hợp ammonia từ nitrogen và hydrogen thuộc loại phản ứng này. Các phản ứng này được gọi là phản ứng gì? Để tăng hiệu suất của chúng, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ,... như thế nào?
Đọc tiếp
Hướng dẫn giải
Thảo luận (1)
H24
Dựa vào phương trình hóa học của phản ứng điều chế khí oxygen từ KMnO4, em hãy cho biết phản ứng có xảy ra theo chiều ngược lại được không?
Hướng dẫn giải
Thảo luận (1)
Trong phản ứng điều chế khí oxygen từ KMnO4, các sản phẩm không tác dụng với nhau để tạo thành chất ban đầu nên phản ứng trên không xảy ra theo chiều ngược lại.
Trả lời bởi Quoc Tran Anh Le
H24
Viết phương trình hóa học của phản ứng một chiều mà em biết.
Hướng dẫn giải
Thảo luận (1)
H24
Phản ứng Cl2 tác dụng với H2O có đặc điểm gì khác với phản ứng nhiệt phân thuốc tím?
Hướng dẫn giải
Thảo luận (1)
Phản ứng Cl2 tác dụng với H2O là phản ứng xảy ra theo hai chiều trái ngược nhau (phản ứng thuận nghịch).
Cl2(g) + H2O(l) ⇌ HCl(aq) + HClO(aq)
Phản ứng nhiệt phân thuốc tím là phản ứng chỉ xảy ra theo chiều từ chất tham gia tạo thành sản phẩm (phản ứng một chiều).
Trả lời bởi Quoc Tran Anh Le
QL
Trên thực tế có các phản ứng sau:
2H2 + O2 → 2H2O (1)
\(2H_2O\underrightarrow{đp}2H_2+O_2\)
Vậy có thể viết:
2H2 + O2 ⇌ 2H2O được không? Tại sao?
Hướng dẫn giải
Thảo luận (1)
Không được viết 2H2 + O2 ⇌ 2H2O vì phản ứng (1) và phản ứng (2) không xảy ra trong cùng một điều kiện:
+ Phản ứng (1) diễn ra trong điều kiện nhiệt độ cao.
+ Phản ứng (2) diễn ra trong quá trình điện phân nước.
Trả lời bởi Quoc Tran Anh Le
H24
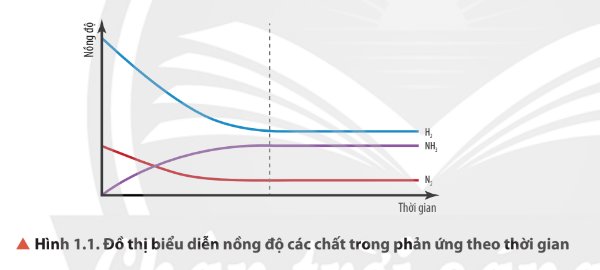
Quan sát Hình 1.1, nhận xét sự biến thiên nồng độ của các chất trong hệ phản ứng theo thời gian (với điều kiện nhiệt độ không đổi).
Hướng dẫn giải
Thảo luận (1)
\(\left[N_2\right],\left[H_2\right]\) giảm, \(\left[NH_3\right]\) tăng.
Sau mốc thời gian nhất định, nồng độ các chất không thay đổi.
Trả lời bởi Khai Hoan Nguyen
H24
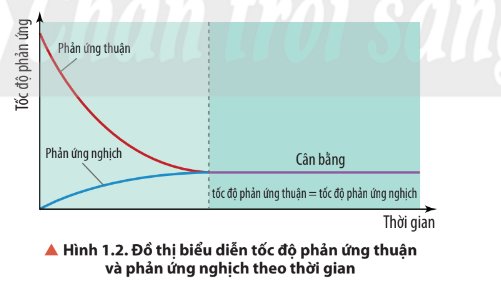
Quan sát Hình 1.2, nhận xét về tốc độ của phản ứng thuận và tốc độ của phản ứng nghịch theo thời gian trong điều kiện nhiệt độ không đổi. Nồng độ các chất trong phản ứng thay đổi như thế nào?
Hướng dẫn giải
Thảo luận (1)
- Ban đầu:
+ Tốc độ phản ứng thuận giảm dần;
+ Tốc độ phản ứng nghịch tăng dần;
- Đến thời điểm cân bằng: Tốc độ phản ứng thuận = tốc độ phản ứng nghịch.
Trả lời bởi GV Nguyễn Trần Thành Đạt
H24
Sử dụng dữ liệu Bảng 1.1, hãy tính giá trị của biểu thức frac{{{rm{(}}{{rm{N}}_{rm{2}}}{{rm{O}}_{rm{4}}}{rm{)}}}}{{{{{rm{(N}}{{rm{O}}_{rm{2}}}{rm{)}}}^{rm{2}}}}} trong 5 thí nghiệm. Nhận xét giá trị thu được từ các thí nghiệm khác nhau.
Đọc tiếp
Sử dụng dữ liệu Bảng 1.1, hãy tính giá trị của biểu thức \(\frac{{{\rm{(}}{{\rm{N}}_{\rm{2}}}{{\rm{O}}_{\rm{4}}}{\rm{)}}}}{{{{{\rm{(N}}{{\rm{O}}_{\rm{2}}}{\rm{)}}}^{\rm{2}}}}}\) trong 5 thí nghiệm. Nhận xét giá trị thu được từ các thí nghiệm khác nhau.
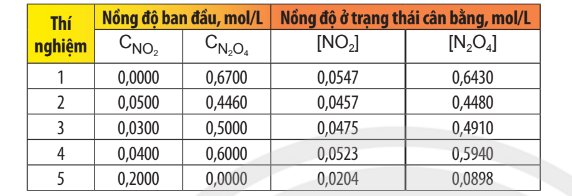
Hướng dẫn giải
Thảo luận (1)
H24
Viết các biểu thức tính tốc độ phản ứng thuận và tốc độ phản ứng nghịch của phản ứng thuận nghịch sau, biết phản ứng thuận và phản ứng nghịch đều là phản ứng đơn giản:
aA+bB ⇌ cC + dD
Lập tỉ lệ giữa hằng số tốc độ phản ứng thuận và hằng số tốc độ phản ứng nghịch ở trạng thái cân bằng.
Hướng dẫn giải
Thảo luận (2)
\(v_{thuận}=k_{thuận}\left[A\right]^a\left[B\right]^b\\ v_{nghịch}=k_{nghịch}\left[C\right]^c\left[D\right]^d\\\dfrac{k_{thuận}}{k_{nghịch}} =\dfrac{\left[C\right]^c\left[D\right]^dv_{thuận}}{\left[A\right]^a\left[B\right]^bv_{nghịch}}\)
Trả lời bởi Khai Hoan Nguyen
H24
Cho hệ cân bằng sau:
2SO2(g) + O2(g) → 2SO3(g)
Viết biểu thức tính hằng số cân bằng KC của phản ứng trên.
Hướng dẫn giải
Thảo luận (1)
\(K_C=\dfrac{\left[SO_3\right]^2}{\left[SO_2\right]^2\left[O_2\right]}\)
Trả lời bởi Khai Hoan Nguyen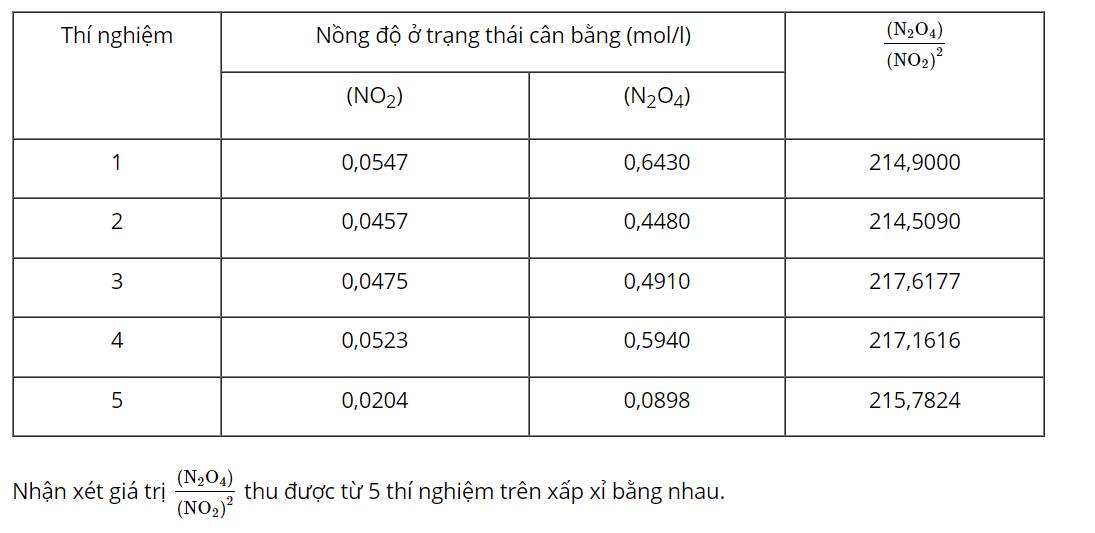
- Trong các phản ứng hoá học, loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu được gọi là phản ứng thuận nghịch.
- Để tăng hiệu suất của chúng, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ,... dựa theo nguyên lí Le Chatelier: “Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động đó”.
Trả lời bởi Quoc Tran Anh Le