- Liên kết σ là sự xen phủ trục
- Liên kết п là sự xen phủ bên
- Liên kết σ là sự xen phủ trục
- Liên kết п là sự xen phủ bên
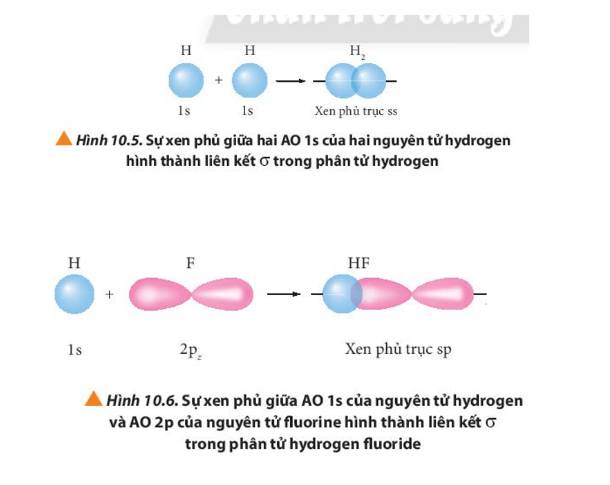
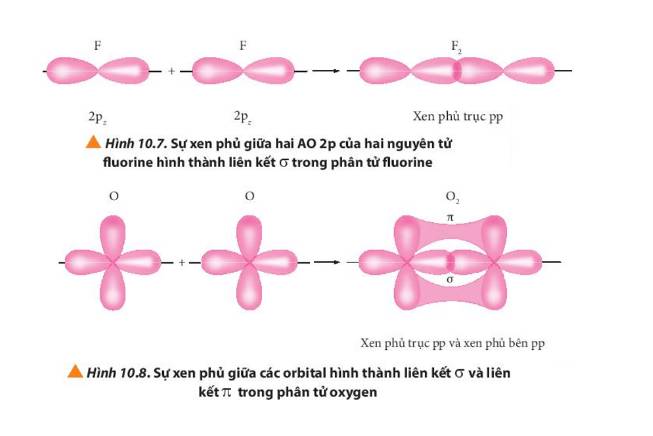
Quan sát các Hình từ 10.5 đến 10.8, cho biết liên kết nào trong mỗi phân tử được tạo thành bởi sự xen phủ trục hoặc xen phủ bên của các orbital.
Mô tả sự tạo thành liên kết trong phân tử chlorine bằng sự xen phủ của các AO.
Vẽ sơ đồ xen phủ orbital giữa 2 nguyên tử carbon hình thành liên kết đôi trong phân tử ethylene (C2H4).
Sự xen phủ có sự tham gia của orbital nào luôn là xen phủ trục?
Cho biết số liên kết σ và liên kết п trong phân tử acetylene (C2H2).
Mô tả sự hình thành liên kết п.
Số liên kết σ và liên kết п trong mỗi liên kết đơn, liên kết đôi và liên kết ba lần lượt bằng bao nhiêu?
Quan sát Hình 10.8, hãy so sánh sự hình thành liên kết σ và liên kết п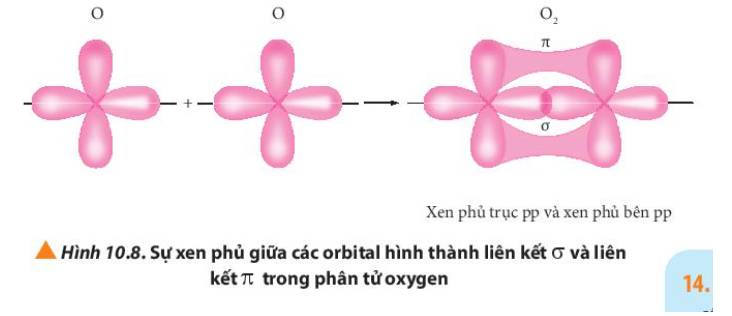
Trong việc hình thành liên kết hóa học, không phải lúc nào các nguyên tử cũng cho, nhận electron hóa trị với nhau như trong liên kết ion. Thay vào đó, chúng có thể cùng nhau sử dụng chung các electron hóa trị để cùng thỏa mãn quy tắc octet. Trong trường hợp này, một loại liên kết hóa học mới được hình thành. Đó là loại liên kết gì?