nHNO3 pư = 4,5 (mol)
Giải thích các bước giải:
Đặt số mol của Cu, Mg, Al lần lượt là a,b,c (mol)
quá trình nhường e
Cu ---> Cu+2 +2e
a -----> 2a (mol)
Mg ---> Mg+2 +2e
b -----> 2b (mol)
Al -----> Al+3 +3e
c -----> 3c (mol)
quá trình nhận e
N+5 +3e ---> N+2 (NO)
0,03<-- 0,01 (mol)
N+5 + 1e ---> N+4 (NO2)
0,04<--- 0,04 (mol)
Bảo toàn e ta có:
ne KIm loại nhường = n e N+5 nhận
=> 2a + 2b + 3c = 0,01 + 0,04
=> 2a + 2b + 3c = 0,05 (mol)
Có: nNO3- (trong muối) = 2nCu(NO3)2 + 2nMg(NO3)2 + 3nAl(NO3)3
= 2a + 2b + 3c
= 0,05 (mol)
BTKL có: m muối = mKL + mNO3- (trong muối)
= 1,35 + 0,05.62
= 4,45 (g)
nHNO3 pư = nNO + nNO2 + nNO3- (trong muối)
= 0,01 + 0,04 + 4,45
= 4,5 (mol)
*tk
Cu, Mg, Al + \(HNO_3\) 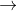 Muối nitrat + NO + \(NO_2\)
Muối nitrat + NO + \(NO_2\)
Bảo toàn điện tích: \(n_{NO_3}\)- (trong muối) = \(3n_{NO}\) + \(n_{NO_2}\) = 0,07 mol
=> Muối = \(m_{MK}\) + \(m_{NO_3}\)- = 1,35 + 0,07.62 = 5,69 g
phần sau dư rồi đâu cần tính số mol HNO3 đâu bạn



