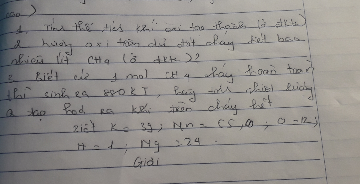1. Đốt cháy hoàn toàn 40g 1 mẩu than có chứa 5% tạp chất không cháy và 20% lưu huỳnh.
a/ Tính thể tích kk cần dùng để đốt cháy mẩu than trên.
b/Tính thể tích các khí tạo thành sau phản ứng.( Các thể tích khí đó ở đktc)
2. 1 oxit đc tạo bởi 2 ngto là sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và oxi là 7/3/ Tìm CTHH của oxit đó.
1. PTHH: \(C+O_2\underrightarrow{t^o}CO_2\\ 2,5mol:2,5mol\rightarrow2,5mol\)
\(S+O_2\underrightarrow{t^o}SO_2\\ 0,25mol:0,25mol\rightarrow0,25mol\)
\(m_C=75\%40=30\left(g\right)\Leftrightarrow n_C=2,5\left(mol\right)\)
\(m_S=20\%40=8\left(g\right)\Leftrightarrow n_S=0,25\left(mol\right)\)
\(n_{O_2}=0,25+2,5=2,75\left(mol\right)\)
\(V_{O_2}=2,75.22,4=61,6\left(l\right)\)
\(V_{kk}=\dfrac{61,6}{20\%}100\%=308\left(l\right)\)
b. \(V_{khi}=\left(2,5+0,25\right)22,4=61,6\left(l\right)\)
2. 1 oxit đc tạo bởi 2 ngto là sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và oxi là 7/3/ Tìm CTHH của oxit đó.
Gọi CTHH của oxit sắt là \(Fe_xO_y\)
Theo đề bài ta có: \(m_{Fe}:m_O=7:3\)
\(\dfrac{m_{Fe}}{m_O}=\dfrac{56x}{16y}=\dfrac{7}{3}\)
\(\Leftrightarrow168x+112y\Leftrightarrow\dfrac{x}{y}=\dfrac{112}{168}=\dfrac{2}{3}\)
Vậy CTHH của oxit sắt là \(Fe_2O_3\)
Bài 2:
Gọi công thức hóa học của oxit là: \(Fe_xO_y\)
Tỉ lệ khối lượng: \(\dfrac{m_{Fe}}{m_O}=\dfrac{56x}{16y}=\dfrac{7}{3}\)
Giải ra ta có: \(\dfrac{x}{y}=\dfrac{1}{1,5}=\dfrac{2}{3}\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\)
Vậy công thức cần tìm của oxit là: \(Fe_2O_3\)