Bài 28: Không khí - Sự cháy
Nội dung lý thuyết
Các phiên bản khácChúng ta có thể dễ dàng suy luận được trong không khí phải có khí oxi để con người và sinh vật có thể thực hiện quá trình hô hấp và tồn tại .Vậy ngoài oxi, trong không khí còn có những khí nào khác? Cách nào để xác định thành phần không khí? Không khí có liên quan gì đến sự cháy? Tại sao khi có gió to đám cháy càng dễ bùng cháy hơn? Làm thế nào để dập tắt đám cháy và tốt hơn là không để đám cháy xảy ra?
I. THÀNH PHẦN CỦA KHÔNG KHÍ
1. Thí nghiệm
Lắp ráp thí nghiệm như hình 1.a. Đun nóng photpho đỏ trên muôi sắt, khi photpho cháy đưa nhanh vào ống nghiệm rồi đồng thời đậy kín miệng ống (hình 1.c)

Phần thể tích còn trống (Từ vạch số 2 đến vạch số 6) của ống nghiệm được dánh dấu và chia làm 5 phần bằng nhau. Khi cho photpho đỏ đang cháy vào trong ống nghiệm, mực nước trong ống nghiệm dâng lên đúng bằng 1/5 phần thể tích còn trống trong ống nghiệm. (vạch 2).
Nhận xét
- Khi đưa photpho đang cháy vào trong ống nghiệm, photpho tác dụng với oxi trong không khí tạo thành khói trắng P2O5 (tan trong nước). Khi oxi trong ống nghiệm tác dụng hết với photpho, áp suất trong bình giảm làm cho mực nước dâng lên đúng bằng 1/5 thể tích phần trống trong ống nghiệm. Chứng tỏ khí oxi chiếm khoảng 1/5 thể tích trong không khí.
- Khí còn lại trong ống chủ yếu là nitơ.
Kết luận
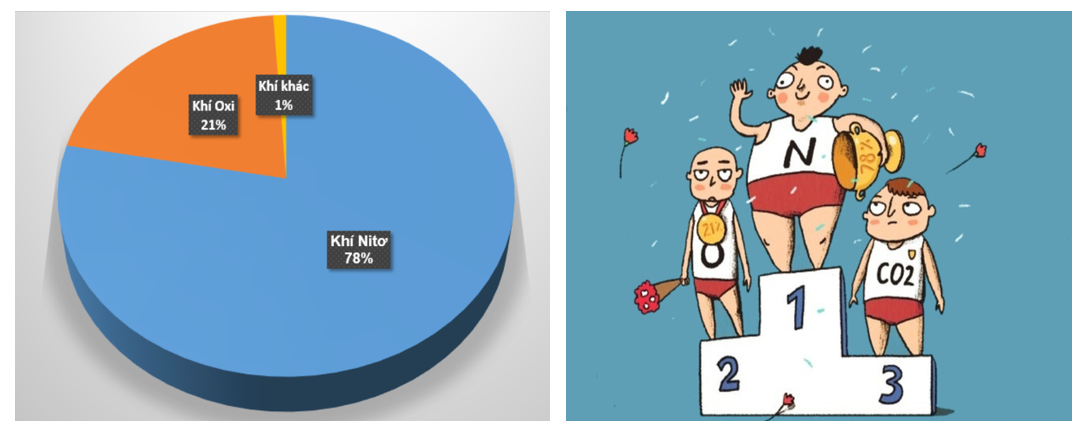
Vậy không khí là một hỗn hợp khí trong đó khí oxi chiếm khoảng 1/5 thể tích, chính xác hơn là khí oxi chiếm 21% thể tích không khí, phần còn lại hầu hết là khí nitơ.
2. Ngoài khí oxi và nitơ, không khí còn chứa khí nào khác?
Quan sát các bề mặt dung dịch nước vôi, cốc nước lạnh người ta thấy trên bề mặt của dung dịch nước vôi để trong không khí lâu ngày sẽ xuất hiện một lớp màng mỏng màu trắng, còn cốc nước lạnh sẽ thấy vài giọt nước nhỏ xung quanh thành cốc (Hình 2).

Nhận xét
Màng trắng xuất hiện trên bề mặt dung dịch nước vôi là vì do khí cacbonic (CO2) đã tác dụng với nước vôi tạo thành kết tủa CaCO3 màu trắng, còn cốc nước lạnh do có nhiệt độ thấp nên đã làm ngưng tụ hơi nước trong không khí, làm cho xung quanh cốc có các giọt nước nhỏ.
Kết luận
Trong không khí ngoài oxi và nitơ còn có khí cacbonic (CO2) và hơi nước (H2O), ngoài ra còn có các khí hiếm như neon (Ne), agon (Ar), khói bụi... Các khí này chỉ chiếm tỉ lệ rất nhỏ trong không khí (khoảng 1%).
3. Bảo vệ không khí trong lành, tránh gây ô nhiễm không khí.
- Không khí bị ô nhiễm, gây ra những tác hại đối với sức khỏe con người, động vật, thực vật,... Không khí bị ô nhiễm các khí như NO2, SO2 sẽ gây lên hiện tượng mưa axit phá hoại, ăn mòn dần các công trình xây dựng như nhà cửa, cầu cống, di tích lịch sử,...
- Nếu nồng độ khí cacbonic thải ra môi trường quá lớn sẽ làm tăng hiệu ứng nhà kính, sự nóng lên toàn cầu, khiến băng tan ở hai cực của trái đất làm cho con người phải chịu các trận thiên tai, lũ lụt thảm khốc.

- Phải xử lí khí thải của các nhà máy, các lò đốt, các phương tiện giao thông, .. để hạn chế đến mức thấp nhất việc đưa vào khí quyển các khí có hại như SO2, CO2, CO, khói bụi,...
- Bảo vệ không khí trong sạch là nhiệm vụ của mỗi người của mỗi quốc gia trên hành tinh chúng ta. Bảo vệ rừng, trồng rừng, trồng cây xanh là những biện pháp tích cực để bảo vệ không khí trong lành.
II. SỰ CHÁY VÀ SỰ OXI HÓA CHẬM
1. Sự cháy
- Sự cháy là sự oxi hóa, có tỏa nhiệt và phát sáng.

@90437@
Sự cháy của một chất trong không khí và trong oxi có gì giống nhau và khác nhau?
Giống nhau: đều là quá trình oxi hóa (sự oxi hóa).
Khác nhau: Sự cháy trong không khí xảy ra chậm hơn, tạo ra nhiệt độ thấp hơn khi cháy trong oxi. Đó là vì trong không khí thể tích nitơ gấp 4 lần thể tích oxi, diện tích tiếp xúc của các chất cháy với các phân tử oxi ít hơn nhiều so với việc đốt trong môi trường toàn là oxi nên sự cháy diễn ra chậm hơn. Một phần nhiệt bị tiêu hao để đốt nóng khí nitơ nên nhiệt độ đạt được thấp hơn.
2. Sự oxi hóa chậm
- Đó là sự oxi hóa có tỏa nhiệt nhưng không phát sáng.
- Sự oxi hóa chậm thưởng xẩy ra trong tự nhiên: đồ vật bằng gang, thép để trong không khí lâu ngày sẽ bị gỉ; thức ăn không được bảo quản tốt thì sẽ bị ôi thiu;…

@90506@
3. Điều kiện phát sinh và các biện pháp để dập tắt sự cháy
Điều kiện phát sinh sự cháy:
- Chất phải nóng đến nhiệt độ cháy.
- Phải có đủ khí oxi để xảy ra cháy.
Muốn dập tắt sự cháy ta phải:
- Hạ nhiệt độ của chất cháy xuống dưới nhiệt độ cháy.
- Cách li chất cháy với khí oxi.
Các biện pháp dập tắt sự cháy:
- Dùng bình cứu hóa, phun nước vào đám cháy, dùng chăn ướt trùm lên ngọn lửa để ngăn đám cháy tiếp xúc với oxi.

III. Tổng kết
1. Không khí gồm 21% là khí oxi, 78% là khí nito, 1% là các khí khác. Mỗi người phải có trách nhiệm giữ cho không khí trong lành.
2. Sự oxi hóa chậm là sự oxi hóa có tỏa nhiệt nhưng không phát sáng.
3. Sự cháy là sự oxi hóa có tỏa nhiệt và phát sáng. Điều kiện để có sự cháy là: chất phải nóng đến nhiệt độ cháy; phải có đủ khí oxi cho sự cháy.
4. Muốn dập tắt sự cháy phải phải thực hiện đủ một hoặc cả hai biện pháp: Hạ nhiệt độ của chất cháy xuống dưới nhiệt độ cháy; cách li chất cháy với oxi.
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
Danh sách các phiên bản khác của bài học này. Xem hướng dẫn
| Nguyễn Trần Thành Đạt đã đóng góp một phiên bản khác cho bài học này (14 tháng 7 2021 lúc 0:48) | 0 lượt thích |