Cho phản ứng sau ở điều kiện chuẩn:
H-H(g) + F-F(g) -> 2H-F(g)
Tính năng lượng cần để phá vỡ các liên kết trong H2, F2 và năng lượng tỏa ra (theo kJ) khi hình thành liên kết trong HF cho phản ứng trên.
Cho phản ứng sau ở điều kiện chuẩn:
H-H(g) + F-F(g) -> 2H-F(g)
Tính năng lượng cần để phá vỡ các liên kết trong H2, F2 và năng lượng tỏa ra (theo kJ) khi hình thành liên kết trong HF cho phản ứng trên.
Xác định số lượng mỗi loại liên kết trong các phân tử trước và sau phản ứng của CH4 với Cl2.
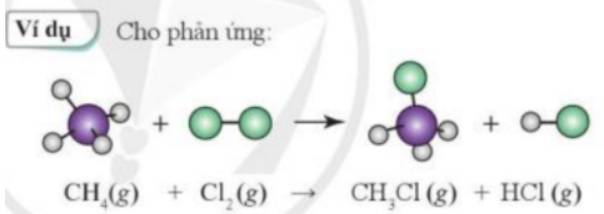
- Trước phản ứng: có 4 liên kết C – H và 1 liên kết Cl – Cl
- Sau phản ứng: Có 3 liên kết C – H, 1 liên kết C – Cl, 1 liên kết H - Cl
Trả lời bởi Hà Quang MinhDựa vào năng lượng liên kết, tính ${\Delta _r},H_{298}^0$ các phản ứng sau:
a) Các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4, C2H6, H2 ở thể khí.
b) F2(g) + H2O(g) → 2HF(g) + ½ O2(g)
Dự đoán các phản ứng trên là thuận lợi hay không thuận lợi.
a)
- Xét phản ứng đốt cháy 1 mol C2H4
C2H4 (g) + 3O2 (g) → 2CO2 (g)+ 2H2O (g)
∆fH0298 = 1 x Eb (C2H4) + 3 x Eb (O2) - 2 x Eb (CO2) - 2 x Eb (H2O)
∆fH0298 = 1 x EC=C + 4 x EC-H + 3 x EO2 – 2 x 2EC=O – 2 x 2EO-H
∆fH0298 = 1x611 + 4x414 + 3x498 – 2x2x799 – 2x2x464 = -1291kJ
- Xét phản ứng đốt cháy 1 mol C2H6
C2H6 (g) + 7/2 O2 (g) → 2CO2 (g)+ 3H2O (g)
∆fH0298 = 1 x Eb (C2H6) + 7/2 x Eb (O2) - 2 x Eb (CO2) - 3 x Eb (H2O)
∆fH0298 = 1 x EC-C + 6 x EC-H + 7/2 x EO2 – 2 x 2EC=O – 3 x 2EO-H
∆fH0298 = 1x347 + 6x414 + 7/2 x498 – 2x2x799 – 3x2x464 = -1406kJ
- Xét phản ứng đốt cháy 1 mol CO
CO(g) + ½ O2 (g) → CO2(g)
∆fH0298 = 1 x Eb (CO) + 1/2 x Eb (O2) - 1 x Eb (CO2)
∆fH0298 = 1 x ECO + 1/2 x EO2 – 1 x 2EC=O
∆fH0298 = 1 x 1072 + 1/2 x 498– 1x2x799 = -277kJ
b)
F2(g) + H2O(g) → 2HF(g) + ½ O2 (g)
∆fH0298 = 1 x Eb (F2) + 1 x Eb (H2O) - 2 x Eb (HF) – 1/2 x Eb (O2)
∆fH0298 = 1 x EF-F + 1x2EO-H - 2 x EH-F - 1/2 x EO2
∆fH0298 = 1 x 159 + 2x464– 2x565 - 1/2 x 498= -292kJ
Các phản ứng trên đều có giá trị elthanpy âm => Các phản ứng trên đều thuận lợi
Trả lời bởi Hà Quang MinhPhản ứng quang hợp là phản ứng thu năng lượng dưới dạng ánh sáng:
6nCO2(g) + 6nH2O(l) → (C6H12O6)n(s) + 6nO2(g)
Hãy tính xem cần phải cung cấp bao nhiêu năng lượng dưới dạng ánh sáng cho phản ứng quang hợp để tạo thành 1 mol glucose C6H12O6(s), biết enthalpy tạo thành chuẩn của chất này là -1271,1 kJ.mol-1. Biến thiến enthalpy tạo thành chuẩn của các chất khác tra ở phụ lục 3, trang 119.
6nCO2(g) + 6nH2O(l) → (C6H12O6)n(s) + 6nO2(g)
∆fH0298 = ∆fH0298 (C6H12O6) + 6 x ∆fH0298 (O2) - 6 x ∆fH0298 (CO2) - 6 x ∆fH0298 (H2O)
= -1271,1 + 6 x 0 – 6 x -393,5 – 6 x -285,8 = 2804,7 kJ.mol-1
=> Phải cung cấp 2804,7 kJ dưới dạng ánh sáng cho phản ứng quang hợp để tạo thành 1 mol glucose C6H12O6(s)
Trả lời bởi Hà Quang MinhCho phản ứng: N2(g) + 3H2(g) → 2NH3(g) ${\Delta _r},H_{298}^0$ = -92,22 kJ.
a) Trong nhà máy sản xuất NH3, ban đầu phải đốt nóng N2 và H2 để phản ứng diễn ra. Nhiệt tỏa ra từ phản ứng này lại được dùng để đốt nóng hỗn hợp N2 và H2 cho quá trình phản ứng tiếp theo. Cách làm này có ý nghĩa gì về khía cạnh kinh tế? Giải thích.
b) Tính enthalpy tạo thành chuẩn của NH3.
a)Phản ứng sản xuất NH3 là phản ứng tỏa nhiệt, lượng nhiệt tỏa ra dùng để đốt nóng hỗn hợp N2 và H2 cho phản ứng tiếp tục xảy ra
=> Tiết kiệm nhiên liệu đốt cho quá trình phản ứng
b) N2(g) + 3H2(g) → 2NH3(g) ${\Delta _r},H_{298}^0$= -92,22 kJ
Ta có: -92,22 = 2 x ∆fH0298 (NH3) – 1 x ∆fH0298 (N2) - 3 x ∆fH0298 (H2)
=> -92,22 = 2 x ∆fH0298 (NH3) – 0 – 0
=> ∆fH0298 (NH3) = -46,11 kJ
Trả lời bởi Hà Quang MinhTính ${\Delta _r},H_{298}^0$ cho phản ứng sau dựa theo năng lượng liên kết.
CH4(g) + X2(g) → CH3X(g) + HX(g)
Với X = F, Cl, Br, I. Liên hệ giữa mức độ phản ứng (dựa theo ${\Delta _r},H_{298}^0$) với tính phi kim (F > Cl > Br > I). Tra các giá trị năng lượng liên kết của Phụ lục 2, trang 118.
- Xét X là F:
CH4(g) + F2(g) → CH3F(g) + HF(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (F2) - 1 x Eb (HF) - x Eb (CH3F)
∆rH0298 = 1 x 4EC-H + 1 x EF-F - 1 x EH-F - 1 x (3EC-H + EC-F)
∆rH0298 = 1x4 x414 + 1x159– 1x565 - 1x(3x414 + 1x485)= -477kJ
- Xét X là Cl:
CH4(g) + Cl2(g) → CH3Cl(g) + HCl(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (Cl2) - 1 x Eb (HCl) - x Eb (CH3Cl)
∆rH0298 = 1 x 4EC-H + 1 x ECl-Cl - 1 x EH-Cl - 1 x (3EC-H + EC-Cl)
∆rH0298 = 1x4 x414 + 1x243– 1x431 - 1 x(3x414 + 1x339)= -113kJ
- Xét X là Br:
CH4(g) + Br2(g) → CH3Br(g) + HBr(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (Br2) - 1 x Eb (HBr) - x Eb (CH3Br)
∆rH0298 = 1 x 4EC-H + 1 x EBr-Br - 1 x EH-Br - 1 x (3EC-H + EC-Br)
∆rH0298 = 1x4 x414 + 1x193– 1x364 - 1 x(3x414 + 1x276)= -33kJ
- Xét X là I:
CH4(g) + I2(g) → CH3I(g) + HI(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (I2) - 1 x Eb (HI) - x Eb (CH3I)
∆rH0298 = 1 x 4EC-H + 1 x EI-I - 1 x EH-I - 1 x (3EC-H + EC-I)
∆rH0298 = 1x4 x414 + 1x151– 1x297 - 1 x(3x414 + 1x240)= 28kJ
=> Từ F đến I, tính phi kim giảm dần nên khả năng tham gia phản ứng giảm dần
Trả lời bởi Hà Quang MinhKhi đun bếp than, củi, để đun nấu nhanh hơn, người ta thường dùng quạt để thổi thêm không khí vào bếp. Cách làm này có làm thay đổi biến thiên enthalpy chuẩn của phản ứng C(s) + O2(g) → CO2(g) không? Giải thích.
Cách làm này chỉ làm tăng tốc độ phản ứng chứ không làm thay đổi biến thiên enthalpy chuẩn của phản ứng
Trả lời bởi Hà Quang Minh
∆r\(H^o_{298}\) = EH-H + EF-F – 2.FH-F
∆r\(H^o_{298}\) = 436 + 159 – 2.565 = -535 kJ
Trả lời bởi Hà Quang Minh