Giải thích xu hướng biến đổi bán kính nguyên tử, nhiệt độ nóng chảy và nhiệt độ sôi của các nguyên tố khí hiếm trong Bảng 11.1.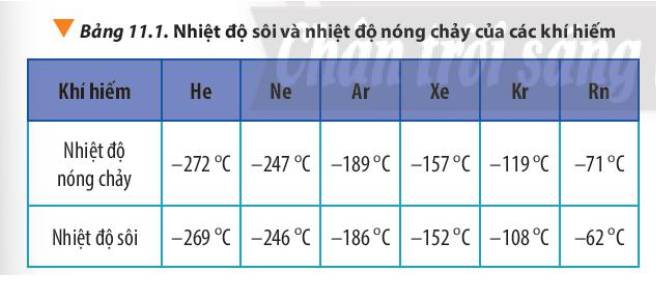
Bài 11: Liên kết hydrogen và tương tác Van der Waals
H24
Hướng dẫn giải
Thảo luận (1)
H24

Tại sao nhện nước có thể di chuyển trên mặt nước?
Hướng dẫn giải
Thảo luận (2)
- Giữa các phân tử nước hình thành lực liên kết hydrogen
=> Liên kết hydrogen giữa các phân tử nước trên bề mặt nước và giữa các phân tử nước trên bề mặt và lớp nước bên dưới tạo ra sức căng bề mặt cho nước
- Chân của con nhện nước gồm các chất kị nước (không phân cực), phân tử các chất nảy đẩy nước khiến cho chân của nhện nước không bị nước bao bọc và tụt xuống dưới nước. Vì vậy chúng có thể di chuyển trên bề mặt nước mà không làm vỡ bề mặt nước
Trả lời bởi Mai Trung Hải Phong
H24
Hợp chất nào dưới đây được liên kết hydrogen liên phân tử
A. CH4
B. H2O
C. PH3
D. H2S
Hướng dẫn giải
Thảo luận (1)
Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N)
=> H2O có thể tham gia liên kết hydrogen liên phân tử
Đáp án B
Trả lời bởi Mai Trung Hải Phong
H24
Sự phân bố electron không đồng đều trong một nguyên tử hay một phân tử hình thành nên
A. một ion dương
B. một ion âm
C. một lưỡng cực vĩnh viễn
D. một lưỡng cực tạm thời
Hướng dẫn giải
Thảo luận (1)
Sự phân bố electron không đồng đều trong một nguyên tử hay một phân tử hình thành nên một lưỡng cực tạm thời
Đáp án D
Trả lời bởi Mai Trung Hải Phong
H24
Khí hiếm nào dưới đây có nhiệt độ sôi thấp nhất?
A. Ne
B. Xe
C. Ar
D. Kr
Hướng dẫn giải
Thảo luận (1)
Trong cùng 1 nhóm, đi từ trên xuống dưới, khối lượng phân tử tăng, kích thước phân tử tăng
=> Tương tác van der Waals tăng
=> Nhiệt độ sôi, nhiệt độ nóng chảy tăng
=> Ne có nhiệt độ sôi thấp nhất
Đáp án A
Trả lời bởi Mai Trung Hải Phong
H24
Biểu diễn liên kết hydrogen giữa các phân tử:
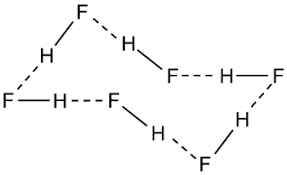
a) Hydrogen fluoride
b) Ethanol (C2H5OH) và nước
Hướng dẫn giải
Thảo luận (2)
a) Hydrogen fluoride: Nguyên tử H của phân tử HF này liên kết với nguyên tử F của phân tử HF khác (biểu diễn bằng 3 nét gạch ---)
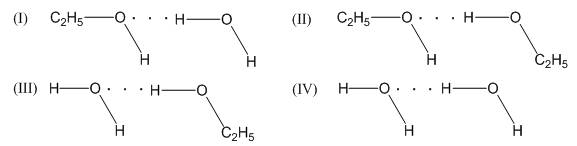
b) Ethanol (C2H5OH) và nước
- Ethanol (C2H5OH) và nước tồn tại 4 kiểu liên kết hydrogen như sau
+ H của C2H5OH liên kết hydrogen với O của H2O (I)
+ H của C2H5OH này liên kết hydrogen với O của C2H5OH khác (II)
+ H của H2O liên kết hydrogen với O của C2H5OH (III)
+ H của H2O này liên kết hydrogen với O của H2O khác (IV)
H24
Trong hai chất ammonia (NH3) và phosphine (PH3), theo em chất nào có nhiệt độ sôi và độ tan trong nước lớn hơn? Giải thích.
Hướng dẫn giải
Thảo luận (2)
Lời giải:
Liên kết P-H không phân cực nên không tạo được liên kết hydrogen giữa các phân tử PH3 với nhau và giữa PH3 với H2O. Mặt khác các phân tử NH3 có thể liên kết với nhau và liên kết với H2O bằng liên kết hydrogen.
⇒ Nhiệt độ sôi và độ tan trong nước của NH3 lớn hơn PH3.
Trả lời bởi Toru
Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất. Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng.
Theo chiều tăng dần của điện tích hạt nhân nguyên tử trong nhóm VIIIA, bán kính nguyên tử tăng đồng thời khối lượng nguyên tử tăng ⇒ Tương tác van der Waals tăng ⇒ Nhiệt độ nóng chảy và nhiệt độ sôi tăng.
Trả lời bởi Mai Trung Hải Phong