Bài 2. Xà phòng và chất giặt rửa
Nội dung lý thuyết
Các phiên bản khácI. Khái niệm, đặc điểm cấu tạo của xà phòng và chất giặt rửa
1. Khái niệm
- Xà phòng: hỗn hợp muối sodium và potassium của acid béo và các chất phụ gia. Thành phần chủ yếu là muối sodium của palmitic acid hoặc stearic acid.
- Chất giặt rửa tổng hợp: các chất được tổng hợp hóa học, có tác dụng giặt rửa như xà phòng nhưng không phải xà phòng, thường là muối sodium alkylsulfate hoặc alkylbenzene sulfonate.
- Chất giặt rửa tự nhiên: sản phẩm từ thiên nhiên có tác dụng giặt rửa (nước quả bồ hòn, quả bồ kết,...).
2. Đặc điểm
Cấu tạo của xà phòng và chất giặt rửa đều gồm hai phần:
- Phần phân cực ("đầu" ưa nước): nhóm carboxylate (xà phòng) hoặc sulfate, sulfonate (chất giặt rửa).
- Phần không phân cực ("đuôi" kị nước): gốc hydrocarbon có mạch dài, không tan trong nước.
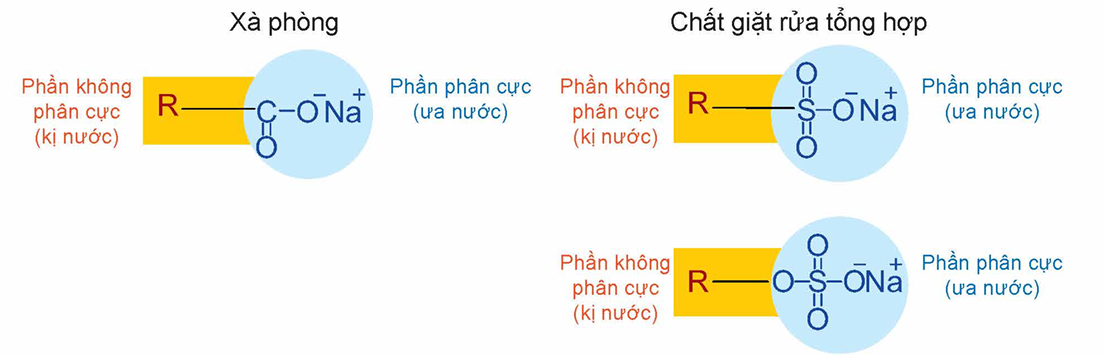
Ví dụ:
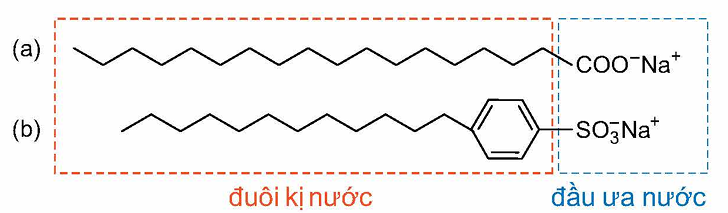
II. Tính chất giặt rửa
- Xà phòng, chất giặt rửa tan vào trong nước ⇒ dung dịch có sức căng bề mặt nhỏ ⇒ vật cần giặt rửa dễ thấm ướt.
- "Đuôi" kị nước thâm nhập vào vết bẩn ⇒ phân chia vết bẩn thành các hạt rất nhỏ có đầu ưa nước quay ra ngoài ⇒ các hạt phân tán vào nước ⇒ bị rửa trôi.
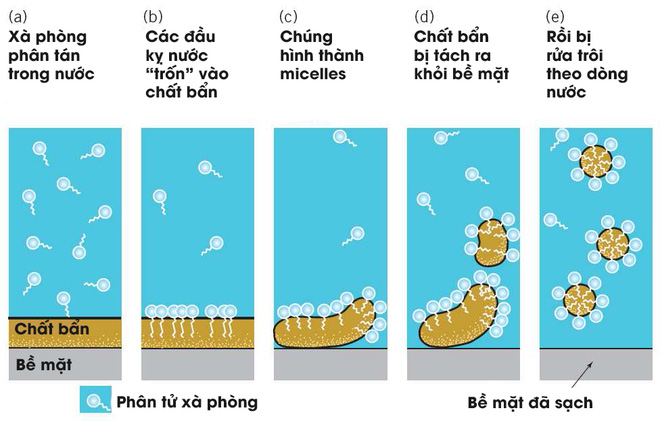
III. Phương pháp sản xuất xà phòng và chất giặt rửa
1. Phương pháp sản xuất xà phòng
- Phản ứng xà phòng hóa:
Chất béo + NaOH/KOH (đặc) → Glycerol + Muối sodium/potassium của acid béo
Ví dụ:
(C17H35COO)3C3H5 + 3NaOH → C3H5(OH)3 + 3C17H35COONa
Muối của acid béo được tách ra, trộn với chất diệt khuẩn, chất tạo hương,... ép thành bánh với nhiều hình dạng khác nhau.
- Từ alkane
Alkane (dầu mỏ) → Acid béo → Muối sodium/potassium của acid béo
2. Phương pháp sản xuất chất giặt rửa tổng hợp
Dầu mỏ → R-SO3H hoặc R-OSO3H → R-SO3Na hoặc R-OSO3Na
Muối sulfonate hoặc muối sulfate được trộn với các chất phụ gia khác nhau ⇒ chất giặt rửa tổng hợp.
IV. Ứng dụng của xà phòng và chất giặt rửa
- Xà phòng dùng để tắm, rửa tay,... Chất giặt rửa tổng hợp dùng để giặt quần áo, rửa chén bát, rửa tay, lau sàn,...
- Ngày nay, chất giặt rửa tổng hợp được sử dụng phổ biến hơn xà phòng do dễ hòa tan trong nước hơn xà phòng và có thể sử dụng với nước cứng, môi trường acid.
- Nhược điểm của chất giặt rửa tổng hợp: khó phân hủy sinh học ⇒ kém thân thiện với môi trường.